有効成分:ゲンタマイシン硫酸塩およびベタメタゾン吉草酸
GENTALYN BETA 0.1%+ 0.1%クリーム
Gentalyn Betaの添付文書は、パックサイズで利用できます。- GENTALYN BETA 0.1%+ 0.1%クリーム
- GENTALYN BETA 0.1%+ 0.05%クリーム
Gentalyn Betaが使用されるのはなぜですか?それはなんのためですか?
薬物療法のカテゴリー
活性コルチコステロイド、抗生物質との組み合わせ。
治療上の適応症
Gentalyn Beta 0.1%+ 0.1%は、二次感染したアレルギー性または炎症性皮膚病の局所治療、または感染の恐れがある場合に適応されます。その使用の適応症は次のとおりです:湿疹(アトピー性、乳児、数)、肛門性器および老人性掻痒症、接触性皮膚炎、脂漏性皮膚炎、神経皮膚炎、三角間、太陽紅斑、剥離性皮膚炎、放射線皮膚炎、うっ血性皮膚炎および乾癬
Gentalynベータを使用すべきでない場合の禁忌
活性物質またはいずれかの賦形剤に対する過敏症。
局所コルチゾンは、皮膚結核および単純ヘルペス、ならびに皮膚局在を伴うウイルス性疾患に苦しむ患者には禁忌です。
使用上の注意GentalynBetaを服用する前に知っておくべきこと
Gentalyn Beta 0.1%+ 0.1%の使用に関連する刺激または感作の場合は、治療を中断し、適切な治療を開始する必要があります。副腎機能低下症を含む、全身性コルチコステロイドについて説明されている望ましくない影響はすべて、特に小児患者において、局所コルチコステロイドでも発生する可能性があります。
局所コルチコステロイドの全身吸収は、大きな皮膚表面の治療または密封包帯の使用により増加します。このような場合、または長期治療が計画されている場合、特に小児患者では、適切な予防措置が必要です。
アミノグリコシド間の交差アレルギー性が実証されています。
局所ゲンタマイシンの全身吸収は、体の広い領域が治療される場合、特に皮膚の損傷が存在する場合、密封包帯法が使用される場合、または治療が長期間計画されている場合に増加します。そのような状況では、それらが発生する可能性があります。望ましくないゲンタマイシンの全身使用で明らかな効果。したがって、特に乳幼児には適切な予防措置を講じる必要があります(以下の「小児科での使用」を参照)。
局所抗生物質の長期使用は、真菌を含む非感受性生物の増殖を可能にすることがあります。この場合、または刺激、感作、または重感染が発生した場合は、ゲンタマイシンによる治療を中止し、特定の治療を開始する必要があります。
相互作用どの薬物または食品がGentalynベータの効果を変更できるか
最近、処方箋のない薬でも、他の薬を服用したことがある場合は、医師または薬剤師に伝えてください。
相互作用の研究は行われていません
警告次のことを知っておくことが重要です。
この薬には、局所アレルギー反応を引き起こす可能性のあるクロロクレゾールとセトステアリルアルコールが含まれています。
小児科での使用:小児患者は、皮膚表面と体重の比率が高いために吸収が大きいため、局所コルチゾンによって誘発される視床下部-下垂体-副腎軸の低下および外因性コルチコステロイドの影響に対して成人よりも敏感であることが判明する可能性があります。
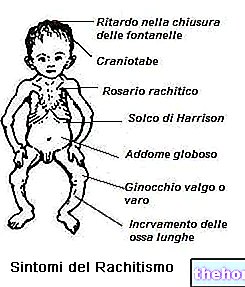
視床下部-下垂体副腎軸のうつ病、クッシング症候群、成長遅延と体重増加、および頭蓋内高血圧は、局所コルチコステロイドで治療された子供で報告されています。子供では、副腎機能低下症の症状には、コルチゾールレベルの低下とACTH刺激への反応の失敗が含まれます。頭蓋内高血圧症には、フォンタネル緊張、頭痛、両側性乳頭浮腫などがあります。
妊娠と母乳育児
妊娠
薬を服用する前に、医師または薬剤師にアドバイスを求めてください。
ステロイド外用薬の安全性は妊婦では確立されていません。したがって、妊娠中は、このクラスに属する薬の使用は、期待される利益が胎児の潜在的なリスクを正当化する場合に限定する必要があります。妊娠中の患者では、これらの薬を集中的に、高用量で、または長期間使用しないでください。
えさの時間
コルチコステロイドの局所投与が母乳中に測定可能な濃度を生成するのに十分な全身吸収をもたらすことができるかどうかは不明であるため、母親にとっての薬物の重要性を考慮して、母乳育児を中止するか治療を中止するかを決定する必要があります。
機械を運転して使用する能力への影響
Gentalyn Beta 0.1%+ 0.1%は、機械を運転または使用する能力に影響を与えません。
Gentalyn Beta 0.1%+ 0.1%は眼科用には使用できません。
いくつかの成分に関する重要な情報。
この薬には、アレルギー反応を引き起こす可能性のあるクロロクレゾールが含まれています。医薬品には、局所的な皮膚反応(接触性皮膚炎など)を引き起こす可能性のあるセトステアリルアルコールも含まれています。
投与量と使用方法Gentalynベータの使用方法:投与量
患部に1日2〜3回少量のクリームを塗ります。
難治性乾癬病変および二次感染深部皮膚病は、以下に説明する密封包帯法と併用すると、コルチコステロイド療法および局所抗生物質によりよく反応する可能性があります。
密封包帯法
- 軽いガーゼの下で病変の表面全体にクリームの厚い層を塗布し、治療領域の端を越えて、透明で防水性と柔軟性のあるプラスチック材料で覆います。
- パッチまたは他の手段で健康な皮膚の端を密封します。
- ドレッシングを1〜3日間そのままにし、必要に応じて手順を3〜4回繰り返します。
この方法では、数日以内に顕著な改善が見られることがよくあります。まれに、毛嚢炎の粟粒性発疹が包帯の下の皮膚に発生し、プラスチックカバーの除去が必要になります。
過剰摂取Gentalynベータを過剰摂取した場合の対処方法
誤ってGentalynBeta 0.1%+ 0.1%を過剰摂取/摂取した場合は、すぐに医師に通知するか、最寄りの病院に行ってください。
Gentalyn Beta 0.1%+ 0.1%の使用について質問がある場合は、医師または薬剤師に相談してください。
症状:局所コルチコステロイドの過剰または長期使用は、副腎下垂体機能を低下させ、二次性副腎機能低下症およびクッシング症候群を含む皮質機能亢進症の症状を引き起こす可能性があります。
ゲンタマイシンの過剰摂取の単一のエピソードは、いかなる症状も引き起こさないはずです。局所ゲンタマイシンの過剰かつ長期の使用は、非感受性の真菌および細菌による病変の形成につながる可能性があります。
治療:適切な対症療法が必要です。急性皮質機能亢進症の症状は通常可逆的です。必要に応じて、電解質の不均衡を治療します。慢性毒性の場合、コルチコステロイドのゆっくりとした除去が推奨されます。真菌や細菌の増殖の場合、「適切な抗真菌または抗菌療法が示されます
副作用Gentalynベータの副作用は何ですか
すべての薬と同様に、Gentalyn Beta 0.1%+ 0.1%は副作用を引き起こす可能性がありますが、誰もがそれらを手に入れるわけではありません。
ゲンタリンベータクリームに対する副作用はほとんど報告されておらず、過敏症、発疹、皮膚の変色などがあります。
局所コルチコステロイドの使用に関連して、特に密封包帯の使用に関連して、以下の望ましくない影響が記載されている:灼熱感、かゆみ、刺激、乾燥肌、毛嚢炎、多毛症、ざ瘡様発疹、色素沈着低下、口周囲皮膚炎、接触性皮膚炎アレルギー、皮膚浸軟、二次感染、皮膚萎縮、脈理およびあせも。
ゲンタマイシン治療は一時的な刺激(紅斑およびかゆみ)を引き起こす可能性があり、通常は治療の中止を必要としません。
パッケージリーフレットに含まれている指示に準拠することで、望ましくない影響のリスクを軽減できます。副作用が深刻になった場合、またはこのリーフレットに記載されていない副作用に気付いた場合は、医師にご相談ください。
有効期限と保持
有効期限:パッケージに記載されている有効期限を参照してください。
警告:パッケージに記載されている有効期限が切れた後は、薬を使用しないでください。表示されている有効期限は、正しく保管された無傷のパッケージに入った製品を指します。
この薬は特別な保管条件を必要としません。
最初の開封後、薬は3ヶ月間有効です。
この薬は子供の手の届かないところに保管してください。
薬は廃水や家庭ごみとして処分しないでください。使用しなくなった薬の処分方法は薬剤師に相談してください。環境保護に役立ちます。
構成
100gのクリームは以下を含みます:有効成分:ゲンタマイシン0.1gに対応する0.166gの硫酸ゲンタマイシン。ベタメタゾン17-吉草酸0.122gは、0.1gのベタメタゾンに相当します。賦形剤:クロロクレゾール、ポリエチレングリコールモノセチルエーテル(Cetomacrogol 1000)、セトステアリルアルコール、白色ワセリン、液体パラフィン、リン酸ナトリウム、リン酸、精製水。
剤形と内容
皮膚用クリーム、30gチューブ。
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
GENTALYNベータクリーム
02.0定性的および定量的組成
ゲンタリンベータ0.1%+ 0.1%クリーム
100gのクリームには、0.166gの硫酸ゲンタマイシン(0.1gのゲンタマイシンに相当)と0.122gの17-吉草酸ベタメタゾン(0.1gのベタメタゾンに相当)が含まれています。
ゲンタリンベータ0.1%+ 0.05%クリーム
100gのクリームには、0.166gの硫酸ゲンタマイシン(0.1gのゲンタマイシンに相当)と0.061gの17-吉草酸ベタメタゾン(0.05gのベタメタゾンに相当)が含まれています。
添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形
クリーム。
04.0臨床情報
04.1治療適応
Gentalyn Beta 0.1%+ 0.1%およびGentalyn Beta 0.1%+ 0.05%は、二次感染したアレルギー性または炎症性皮膚病の局所治療、または感染の恐れがある場合に適応されます。それらの使用の適応症は、湿疹(アトピー性、乳児、数)、肛門性器および老人性掻痒症、接触性皮膚炎、脂漏性皮膚炎、神経皮膚炎、三角間、太陽紅斑、剥離性皮膚炎、放射線皮膚炎、うっ血性皮膚炎および乾癬である。
Gentalyn Beta 0.1%+ 0.05%は、Gentalyn Beta 0.1%+ 0.1%で十分な改善が得られた後、重度または抵抗性の皮膚病の維持療法で特に示されます。体の広い領域または長期の治療を必要とする慢性的な領域。
04.2投与の形態と方法
患部に1日2〜3回少量のクリームを塗ります。
難治性乾癬病変および二次感染深部皮膚病は、以下に説明する密封包帯法と併用すると、コルチコステロイド療法および局所抗生物質によりよく反応する可能性があります。
密封包帯法
1.軽いガーゼの下で病変の表面全体にクリームの厚い層を塗布し、治療領域の端を越えて、透明で防水性があり柔軟なプラスチック材料で覆います。
2.パッチまたは他の手段で健康な皮膚の端を密封します。
3.ドレッシングを1〜3日間そのままにし、必要に応じて手順を3〜4回繰り返します。
この方法では、数日以内に顕著な改善が見られることがよくあります。まれに、毛嚢炎の粟粒性発疹が包帯の下の皮膚に発生し、プラスチックカバーの除去が必要になります。
04.3禁忌
活性物質またはセクション6.1に記載されている賦形剤のいずれかに対する過敏症。
局所コルチゾンは、皮膚結核および単純ヘルペス、ならびに皮膚局在を伴うウイルス性疾患に苦しむ患者には禁忌です。
04.4使用に関する特別な警告と適切な注意事項
Gentalyn Beta 0.1%+ 0.1%またはGentalyn Beta 0.1%+ 0.05%の使用に関連する刺激または感作の場合は、治療を中断し、適切な治療を開始する必要があります。副腎機能低下症を含む、全身性コルチコステロイドについて説明されている望ましくない影響はすべて、特に小児患者において、局所コルチコステロイドでも発生する可能性があります。
アミノグリコシド間の交差アレルギー性が実証されています。
局所コルチコステロイドの全身吸収は、大きな皮膚表面の治療または密封包帯の使用により増加します。このような場合、または長期治療が計画されている場合、特に小児患者では、適切な予防措置が必要です。
局所ゲンタマイシンの全身吸収は、体の広い領域が治療される場合、特に皮膚の損傷が存在する場合、密封包帯法が使用される場合、または治療が長期間計画されている場合に増加します。そのような状況では、それらが発生する可能性があります。望ましくないゲンタマイシンの全身使用で明らかな効果。したがって、特に乳幼児には適切な予防措置を講じる必要があります(以下の「小児科での使用」を参照)。
局所抗生物質の長期使用は、真菌を含む非感受性生物の増殖を可能にすることがあります。この場合、または刺激、感作、または重感染が発生した場合は、ゲンタマイシンによる治療を中止し、特定の治療を開始する必要があります。
小児人口
小児患者は、皮膚表面と体重の比率が高いために吸収が大きいため、局所コルチゾンによって誘発される視床下部-下垂体-副腎軸の低下および外因性コルチコステロイドの影響に対して成人よりも敏感であることがわかる場合があります。
視床下部-下垂体-副腎軸のうつ病、クッシング症候群、成長遅延と体重増加、頭蓋内高血圧は、局所コルチコステロイドで治療された子供で報告されています。子供では、副腎機能低下症の症状には、低レベルのコルチゾール血症と刺激への反応の失敗が含まれます。 ACTHを伴う頭蓋内高血圧の症状には、フォンタネルの緊張、頭痛、および両側性乳頭浮腫が含まれます。
Gentalyn Beta 0.1%+ 0.1%およびGentalyn Beta 0.1%+ 0.05%は眼科用には使用できません。
04.5他の医薬品との相互作用および他の形態の相互作用
相互作用の研究は行われていません。
04.6妊娠と授乳
妊娠
ステロイド外用薬の安全性は妊婦では確立されていません。したがって、妊娠中は、このクラスに属する薬の使用は、期待される利益が胎児への潜在的なリスクを正当化する場合に限定する必要があります。妊娠中の患者では、これらの薬を集中的に、高用量で、または長期間使用しないでください。 。
えさの時間
コルチコステロイドの局所投与が母乳中に測定可能な濃度を生成するのに十分な全身吸収をもたらすことができるかどうかは不明であるため、母親にとっての医薬品の重要性を考慮して、母乳育児を中止するか治療を中止するかを決定する必要があります。
04.7機械の運転および使用能力への影響
Gentalyn Beta 0.1%+ 0.1%およびGentalyn Beta 0.1%+ 0.05%は、機械の運転または使用の能力に影響を与えません。
04.8望ましくない影響
ゲンタリンベータクリームに対する副作用はほとんど報告されておらず、過敏症、発疹、皮膚の変色などがあります。
局所コルチコステロイドの使用に関連して、特に密封包帯の使用に関連して、以下の望ましくない影響が記載されている:灼熱感、かゆみ、刺激、乾燥肌、毛嚢炎、多毛症、ざ瘡様発疹、色素沈着低下、口周囲皮膚炎、接触性皮膚炎アレルギー、皮膚浸軟、二次感染、皮膚萎縮、脈理およびあせも。
ゲンタマイシン治療は一時的な刺激(紅斑およびかゆみ)を引き起こす可能性があり、通常は治療の中止を必要としません。
疑わしい副作用の報告
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスク比を継続的に監視できるため重要です。医療専門家は、イタリア医薬品庁を通じて疑わしい副作用を報告するよう求められます。 、ウェブサイト:https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse。
04.9過剰摂取
症状:局所コルチコステロイドの過剰または長期使用は、下垂体-副腎機能を低下させ、二次性副腎機能低下症およびクッシング症候群を含む高皮質症の症状を引き起こす可能性があります。
ゲンタマイシンの過剰摂取の単一のエピソードは、いかなる症状も引き起こさないはずです。局所ゲンタマイシンの過剰かつ長期の使用は、非感受性の真菌および細菌による病変の形成につながる可能性があります。
処理:適切な対症療法が必要です。急性皮質機能亢進症の症状は通常可逆的です。必要に応じて、電解質の不均衡を治療します。慢性毒性の場合、コルチコステロイドのゆっくりとした除去が推奨されます。真菌や細菌の増殖の場合、「適切な抗真菌または抗菌療法が示されます。
05.0薬理学的特性
05.1薬力学的特性
薬物療法グループ:活性コルチコステロイド、抗生物質との組み合わせ。
ATCコード:D07CC01
Gentalyn Beta 0.1%+ 0.1%およびGentalyn Beta 0.1%+ 0.05%は、局所ゲンタマイシンの広域抗菌効果と、ベタメタゾン17吉草酸の抗炎症作用、抗アレルギー作用、およびかゆみ止め作用を組み合わせたものです。
2つの成分の治療効果を以下に別々に説明します。
ゲンタマイシンはミクロモノスポラ・プルプレアの発酵によって生成され、水に溶けて熱に安定な白色の無定形粉末として得られます。
Schering CorporationU.S.A。の研究所で分離されたこの広域抗生物質皮膚の一次および二次細菌感染症の局所治療に非常に効果的であることが示されています。
ゲンタマイシンに感受性のある細菌には、黄色ブドウ球菌(コアグラーゼ陽性、コアグラーゼ陰性、およびペニシリナーゼ産生菌)、グラム陰性菌、緑膿菌、アエロバクターアエロゲネス、大腸菌、尋常性プロテウス、および肺炎桿菌が含まれます。
クリニックで実施された皮膚反応試験の結果は、ゲンタマイシンが主要な刺激物ではないことを示しています。さらに、ゲンタマイシンは皮膚感作指数が低い。
ベタメタゾン17吉草酸は、コルチコステロイド療法に反応する皮膚病の局所治療に非常に効果的です。
炎症反応の抑制は、そう痒症、紅斑および浸潤の迅速かつ長期の制御をもたらします。
引っかき傷の減少は、病変の悪化および二次感染の発症の可能性を減少させます。
コルチコステロイドに敏感なさまざまな限局性および全身性疾患で実施された臨床研究は、ベタメタゾン17吉草酸が大多数の患者でより迅速で効果的な反応を引き起こすことを示しています。
05.2薬物動態特性
局所コルチコステロイドの経皮吸収は一般にごくわずかですが、大きな皮膚表面を治療したり、密封包帯法を使用したりすると、吸収が増加する可能性があります。
小児では、通常、経皮吸収が高く、ゲンタマイシンの経皮吸収は通常ありません。
05.3前臨床安全性データ
水溶液中のゲンタマイシンを使用したマウスの急性毒性試験では、次のLD50が得られました:皮下485 mg / kg、腹腔内430 mg / kg、静脈内75 mg / kg、経口> 9050 mg / kg。吉草酸ベタメタゾンのLD50をマウスとラットで調べたところ、次の結果が得られました。マウスの経口投与量4210 mg / kg、s.c。 518 mg / kg、i.p。 673 mg / kg;経口ラット100mg / kg。ゲンタマイシンと吉草酸ベタメタゾンは、発がん性が知られている化合物と構造的に類似していません。慢性毒性試験および臨床試験では、発がん性を示唆する可能性のある現象が強調されたことはありません。
クリニックで実施された皮膚反応試験の結果は、ゲンタマイシンが主要な刺激物ではないことを示しています。さらに、ゲンタマイシンは皮膚感作指数が低い。
06.0医薬品情報
06.1添加剤
クロロクレゾール、モノエチレングリコールポリエチレングリコール(セトマクロゴール1000)、セトステアリルアルコール、白色ワセリン、液体パラフィン、リン酸ナトリウム、リン酸、精製水。
06.2非互換性
関係ありません。
06.3有効期間
無傷の包装で2年。
最初の開封後:Gentalyn Beta 0.1%+ 0.1%クリームは3か月間有効です。
06.4保管に関する特別な注意事項
Gentalyn Beta 0.1%+ 0.1%クリーム:この薬は特別な保管条件を必要としません。
Gentalyn Beta 0.1%+ 0.05%クリーム:25°C以上で保管しないでください。
06.5即時包装の性質および包装の内容
Gentalyn Beta 0.1%+ 0.1%クリーム:30gチューブ
Gentalyn Beta 0.1%+ 0.05%クリーム:20gチューブ
06.6使用および取り扱いに関する指示
特別な指示はありません。
07.0マーケティング承認保持者
MSD Italia S.r.l.
ヴィトルキアーノ経由、151
00189ローマ
販売店:
エセックスイタリアS.r.l.
ヴィトルキアーノ経由、151
00189ローマ
08.0マーケティング承認番号
ゲンタリンベータ0.1%+ 0.1%クリームAIC 021736020
ゲンタリンベータ0.1%+ 0.05%クリームAIC 021736032
09.0最初の承認または承認の更新の日付
最初の承認日:1970年4月16日
最新の更新日:2010年6月1日
10.0本文の改訂日
2015年7月













.jpg)