有効成分:フェノバルビタール
GARDENALE 50mg錠
GARDENALE 100mg錠
なぜガーデナーレが使われるのですか?それはなんのためですか?
薬物療法のカテゴリー
抗てんかん薬バルビツール酸塩
治療上の適応症
ガーデナーレは、特にてんかんおよび長期の鎮静を必要とするすべての状態に関して、主に一般的な鎮静剤として示されます。ガーデナーレは、大発作および限局性皮質発作の強直間代発作に特に有用です。慢性バービタール症の無害化。
Gardenaleを使用しない場合の禁忌
活性物質、他のバルビツール酸塩、賦形剤のいずれか、ポルフィリン症、腎不全および肝不全、重度の心臓病、アルコールによる急性中毒、鎮痛薬、催眠薬に対する過敏症。
使用上の注意ガーデナーレを服用する前に知っておくべきこと
フェノバルビタールは中毒性があります。継続的な治療は、抗凝固剤、いくつかの抗生物質、副腎ステロイドなどのいくつかの薬物の代謝を加速する肝酵素の産生を誘発します。
アルコールの効果が高まり、アルコール飲料の摂取を制限する必要があります。
他の向精神薬や抗ヒスタミン薬との関連は、相互作用による予期しない望ましくない影響を避けるために、医師の側で特別な注意と警戒が必要です。
Hypericum perforatum製剤は、血漿レベルの低下とフェノバルビタールの治療効果の低下のリスクがあるため、フェノバルビタールを含む医薬品と併用しないでください(相互作用を参照)。
てんかん患者の治療を突然中止すると、てんかん重積状態を引き起こす可能性があります。
腎不全、肝不全(肝性脳症のリスクのために、生物学的防除を確立する)の場合、高齢者およびアルコール依存症の場合は、投与量を減らしてください。
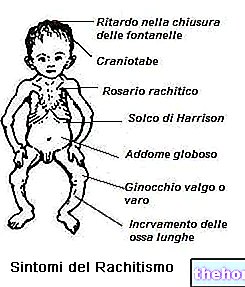
フェノバルビタールによる長期治療を受けている子供では、くる病の予防的治療との関連を考慮する必要があります。
次の生命を脅かす皮膚反応がGardenaleの使用で報告されています:スティーブンス・ジョンソン症候群(SJS)および中毒性表皮壊死症(TEN)。
患者は徴候と症状を知らされ、皮膚反応を注意深く監視されるべきです。 SJSとTENを発症するリスクが最も高いのは、治療の最初の数週間です。
SJSまたはTENの症状または徴候が発生した場合(たとえば、水疱または粘膜病変を伴う進行性の皮膚発疹)、Gardenaleを中止する必要があります。
SJSとTENの管理における最良の結果は、早期診断と疑わしい薬物による治療の即時中止で得られます。早期中止は、より良い予後と関連しています。
患者がGardenaleを使用してSJSまたはTENを発症した場合、Gardenaleはこの患者には使用しないでください。
相互作用どの薬や食品がガーデナーレの効果を変えることができるか
関連付けは推奨されません
エストロゲンとプロゲストゲン(避妊薬として使用)):肝臓の異化作用の増加による避妊効果の低下。できれば、別の避妊法、特に機械的な方法を使用してください。
アルコール:フェノバルビタールの鎮静作用を増強します。治療中はアルコール飲料やアルコールを含む薬を飲まないでください。
オトギリソウ: フェノバルビタールの有効性は、セイヨウオトギリソウベースの製剤の同時投与によって低下する可能性があります。これは、セイヨウオトギリソウベースの製剤による薬物代謝に関与する酵素の誘導によるものであり、したがって、フェノバルビタールと併用して投与すべきではありません。誘導効果は、セイヨウオトギリソウ製品による治療を停止した後、少なくとも2週間持続する可能性があります。
患者がHypericumperforatum製品を同時に服用している場合は、血中フェノバルビタールレベルを監視し、Hypericumperforatum製品による治療を中止する必要があります。血中フェノバルビタールレベルは、セイヨウオトギリソウを止めると増加する可能性があります。フェノバルビタールの投与量を調整する必要があるかもしれません。
特別な注意が必要な協会
シクロスポリン:関連中の活動の減少(異化作用の加速)に伴う循環速度の低下の可能性。逆に、インデューサーの中止後は血漿レベルが上昇します。血漿レベルを制御しながらシクロスポリンの投与量を増やします。インデューサーの中止後は投与量を減らします。
コルチコイド (グルコ、ミネラル、一般的に):コルチコイドの有効性の低下(異化作用の増加)。アディソン人と移植の場合、結果は特に重要です。
臨床的および生物学的防除:関連中および誘導物質の停止後のコルチコイド投与量の適応。
ドキシサイクリン:ドキシサイクリンの血漿中半減期の減少とその結果としての肝代謝の増加におそらく続発するドキシサイクリンの血漿中濃度の減少。
臨床管理および治療計画の可能な適応(1日量を増やすか、1日2回の投与に分割する)。
ハイドロキニジン、キニジン:キニジンの血漿レベルの低下と抗不整脈効果(肝代謝の増加)。
臨床管理、ECG、そしておそらくキニジン血症;必要に応じて、インデューサーによる治療中および中止後のキニジンの投与量を調整します(キニジンの過剰摂取のリスク)。
レボチロキシン:フェニトイン、リファンピシン、カルバマゼピンについて記載されている効果。 T3およびT4の異化作用の増加による甲状腺機能低下症患者の臨床的甲状腺機能低下症のリスク。 T3およびT4の血清レベルを確認し、必要に応じて、インデューサーによる治療中およびその懸濁後にレボチロキシンの投与量を調整します。
テオフィリン (および外挿により、テオフィリンの誘導体):血漿速度およびテオフィリンの活性の低下(酵素誘導によるその代謝の増加)。
臨床および必要に応じてテオフィリンモニタリング。必要に応じて、インデューサーによる治療中およびその懸濁後にテオフィリンの投与量を調整します。
葉酸: 葉酸投与の場合、活性の低下につながる可能性のある血漿フェノバルビタールレベルの低下(葉酸欠乏のために以前に低下した代謝の正常に戻る)。おそらく血漿レベルの臨床的管理および必要に応じて、葉酸の投与中およびその懸濁後のフェノバルビタールの投与量の適応。
バルプロ酸:鎮静(肝異化の阻害)の開始に伴うフェノバルビタールの血漿濃度の増加、子供でより頻繁に。併用療法の最初の15日間の臨床管理と、鎮静の兆候が現れたときのフェノバルビタール投与量の削減。必要に応じて、フェノバルビタールの血漿レベルを確認してください。
経口抗凝固薬: 経口抗凝固薬の効果の低下(肝異化作用の増加)。
フェノバルビタールによる治療中および中止後8日間のプロトロンビンレベルのより頻繁なモニタリングおよび経口抗凝固薬投与量の調整。
イミプラミン抗うつ薬:イミプラミン系抗うつ薬は、全身性発作の発症を助長します。
抗てんかん薬の臨床管理と最終的な投与量の増加。
ジギトキシン:ジギトキシンの効果の減少(肝臓の異化作用の増加)。
臨床管理、ECG、そしておそらくデジトキシン血症。必要に応じて、併用中およびフェノバルビタール離脱後のジギトキシンの投与量調整が望ましい-肝臓での代謝が少ないジゴキシン-プロガビド:血漿フェノバルビタールレベルの上昇の可能性。血漿プロガビドレベルの低下の可能性(検証されていない)臨床管理およびおそらくフェノバルビタールの血漿レベル。
注意して実装される関連付け
カルバマゼピン:これが抗てんかん活性に悪影響を与えることなく、血漿カルバマゼピンレベルの漸進的な減少。特に血漿レベルを解釈する際に考慮されるべきである。
ジソピラミド:ジソピラミドの血漿レベルの低下による抗不整脈効果の低下。
他の中枢神経抑制薬:抗うつ薬(A選択的MAOIを除く)、ほとんどの抗H1抗ヒスタミン薬、クロニジンおよびクロニジン様ベンゾジアゼピン、催眠薬、モルヒネ誘導体(鎮痛薬および抗精神病薬)、神経弛緩薬、ベンゾジアゼピン以外の鎮静剤。中枢神経抑制の増加。これは、特に運転中または機械の使用時に深刻な結果をもたらす可能性があります。
フェニトイン:フェノバルビタールとの関連の場合、予測できない変動が発生する可能性があります:フェニトインの血漿レベルは、抗けいれん作用に悪影響を与えることなく、より頻繁に減少します(代謝の増加)。フェノバルビタールが中断されると、フェニトインの毒性作用が現れることがあります。フェニトインの血漿レベルが上昇します(競争による代謝の阻害)。血漿レベルを解釈する際に考慮されるべきです。
アルプレノロール、メトプロロール、プロプラノロール(ベータ遮断薬): それらの臨床効果の減少(それらの肝代謝の増加)に伴うこれらのベータ遮断薬の血漿レベルの減少。主に肝臓の生体内変化によって排除されるこれらのベータ遮断薬を考慮に入れること。
警告次のことを知っておくことが重要です。
ガーデナーレなどの抗てんかん薬で治療されている少数の患者は、自傷行為や自殺の考えを持っています。そのような考えが生じたときはいつでも、すぐにあなたの医者に連絡してください。
機械を運転して使用する能力への影響
フェノバルビタールによる治療は、注意力を低下させ、反射の時間を長くします。患者は、危険性のために車両の運転や警戒の完全性を必要とする活動を行わないように、これについて警告する必要があります。
妊娠と母乳育児
妊娠する可能性のある患者または出産可能年齢の患者には、専門家のアドバイスを与える必要があります。患者が妊娠を計画している場合は、抗てんかん治療の必要性を再評価する必要があります。
先天性欠損症のリスクは、抗てんかん薬で治療された母親の子孫で2〜3倍に増加します。最も頻繁に報告されているのは、口唇裂、心血管奇形、神経管欠損症です。
抗てんかん薬による多剤療法は、単剤療法よりも先天性奇形のリスクが高い可能性があります。したがって、可能な限り単剤療法を実施することが重要です。
発作が再開する危険性があるため、抗てんかん薬治療の突然の中止は、母親と赤ちゃんの両方に深刻な結果をもたらす可能性があるため、実施すべきではありません。
授乳中のフェノバルビタールの使用はお勧めしません。
投与量と使用方法Gardenaleの使用方法:投与量
1日あたり50から100mgの鎮静剤として。抗けいれん薬として、成人では1日あたり100〜300 mgを2〜3回投与します。
年齢と体重に応じて20〜100mgの子供。
就寝1時間前の「夕方1時間に50〜200mgの重度の不眠症」。
錠剤は少量の水に溶かすか、場合によっては食品に加えることができます。
高齢患者の治療では、医師がポソロジーを注意深く確立する必要があります。医師は、上記の投与量の削減の可能性を評価する必要があります。
過剰摂取あなたがガーデナーレを飲みすぎた場合の対処法
急性バルビツール酸中毒の治療は、患者の状態が許せば、即時の胃洗浄を伴います。すでに吸収された薬物の除去は、強制的な利尿と尿のアルカリ化によって達成することができます。重症の場合、血液透析が有用であり、呼吸を機械的に制御する必要があるかもしれません。肺の合併症を避けるために抗生物質の投与が必要です。
副作用Gardenaleの副作用は何ですか
鎮静、運動失調、眼振および精神錯乱は、特に高齢者において、高用量の投与後に発生する可能性があります。まれな皮膚アレルギー症状。
ビタミンK療法に敏感な低プロトロンビン血症は、フェノバルビタールで治療された母親の新生児に発生する可能性があります。
慢性治療中に、ビタミンD治療に反応する葉酸感受性巨赤芽球性貧血および骨軟化症が発生する可能性があります。
デュピュイトラン拘縮の症例はめったに報告されていません。
- 皮膚:スティーブンス・ジョンソン症候群(SJS)や中毒性表皮壊死症(TEN)などの重度の皮膚副作用(SCAR)が報告されています(使用上の注意を参照)。頻度:非常にまれです。まれな紅斑の症例が報告されています。多面的です。
- 肝胆道i:毒性肝炎のまれな症例。
- 血液学的:白血球減少症、無顆粒球症、血小板減少症および紫斑病のまれな症例。
- 中枢神経系:一部の被験者では、まれにしか発生しない可能性があります:興奮、興奮、せん妄。多動性の症状は、小児患者で発生する可能性があります。
筋骨格系および結合組織障害
ガーデナーレによる長期治療を受けている患者では、骨塩密度の低下、骨減少症、骨粗鬆症、骨折が報告されています。 Gardenaleが骨代謝に影響を与えるメカニズムは特定されていません。
パッケージリーフレットに含まれている指示に準拠することで、望ましくない影響のリスクを軽減できます。添付文書に記載されていない場合でも、望ましくない影響がある場合は医師または薬剤師に通知することが重要です。
有効期限と保持
30°Cを超えない温度で保管してください
有効期限:パッケージに印刷されている有効期限を確認してください。
表示されている有効期限は、無傷で正しく保管されたパッケージに入った製品を指します。
警告:パッケージに記載されている有効期限が切れた後は、薬を使用しないでください。
この薬は子供の手の届かないところに保管してください
構成
GARDENALE 50mg錠
1錠に含まれるもの:
有効成分:フェノバルビタール50 mg
賦形剤:コーンスターチ、ステアリン酸マグネシウム、アルファ化コーンスターチ
GARDENALE 100mg錠
1錠に含まれるもの:
有効成分:フェノバルビタール100 mg
賦形剤:コーンスターチ、ステアリン酸マグネシウム、アルファ化コーンスターチ。
剤形と内容
経口用錠剤。
- ブリスターに50mgの30錠の箱
- ブリスターパックに入った100mgの20錠の箱
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
GARDENALE
02.0定性的および定量的組成
GARDENALE 50mg錠
1錠に含まれるもの:
有効成分: フェノバルビタール50mg。
GARDENALE 100mg錠
1錠に含まれるもの:
有効成分:フェノバルビタール100mg。
添加剤については、6.1を参照してください
03.0剤形
タブレット。
04.0臨床情報
04.1治療適応
ガーデナーレは、特にてんかんおよび長期の鎮静を必要とするすべての状態に関して、主に一般的な鎮静剤として示されます。ガーデナーレは、大発作および限局性皮質発作の強直間代発作に特に有用です。慢性からの解毒に使用できます。バービチュリズム。
04.2投与の形態と方法
1日あたり50から100mgの鎮静剤として。抗けいれん薬として、成人では1日あたり100〜300 mgを2〜3回投与します。
年齢と体重に応じて20〜100mgの子供。
錠剤は少量の水に溶かすか、場合によっては食品に加えることができます。高齢患者の治療では、医師がポソロジーを注意深く確立する必要があります。医師は、上記の投与量の削減の可能性を評価する必要があります。
04.3禁忌
活性物質、他のバルビツール酸塩または賦形剤のいずれかに対する過敏症、ポルフィリン症、腎および肝不全、重度の心臓病、アルコールによる急性中毒、鎮痛薬、催眠薬。
04.4使用に関する特別な警告と適切な注意事項
さまざまな適応症で抗てんかん薬を服用している患者で、自殺念慮と行動の症例が報告されています。ランダム化臨床試験とプラセボのメタアナリシスでも、自殺念慮と行動のリスクがわずかに増加していることが明らかになりました。
このリスクのメカニズムは確立されておらず、入手可能なデータは、Gardenaleによるリスク増加の可能性を排除していません。
したがって、患者は自殺念慮と行動の兆候がないか監視されるべきであり、もしそうなら適切な治療が考慮されるべきです。患者(および介護者)は、自殺念慮または自殺行動の兆候が現れた場合、治療を行う医師に通知するように指示する必要があります。
次の生命を脅かす皮膚反応がGardenaleの使用で報告されています:スティーブンス・ジョンソン症候群(SJS)および中毒性表皮壊死症(TEN)。
患者は徴候と症状を知らされ、皮膚反応を注意深く監視されるべきです。 SJSとTENを発症するリスクが最も高いのは、治療の最初の数週間です。
SJSまたはTENの症状または徴候が発生した場合(たとえば、水疱または粘膜病変を伴う進行性の皮膚発疹)、Gardenaleを中止する必要があります。
SJSとTENの管理における最良の結果は、早期診断と疑わしい薬物による治療の即時中止で得られます。早期中止は、より良い予後と関連しています。
患者がGardenaleを使用してSJSまたはTENを発症した場合、Gardenaleはこの患者には使用しないでください。
腎不全、肝不全(肝性脳症のリスクのために、生物学的防除を確立する)の場合、高齢者およびアルコール依存症の場合は、投与量を減らしてください。
相互作用が強化されているため、治療中のアルコール飲料はお勧めしません。
フェノバルビタールによる長期治療を受けている子供では、くる病の予防的治療との関連を考慮する必要があります:ビタミンD2または25OH-ビタミンD3。
また、4.5、4.6、4.7項も注意深く読んでください。
フェノバルビタールは中毒性があります。継続的な治療は、抗凝固剤、いくつかの抗生物質、副腎ステロイドなどのいくつかの薬物の代謝を加速する肝酵素の産生を誘発します。
他の向精神薬や抗ヒスタミン薬との関連は、相互作用による予期しない望ましくない影響を避けるために、医師の側で特別な注意と警戒が必要です。
Hypericum perforatum製剤は、血漿レベルの低下とフェノバルビタールの治療効果の低下のリスクがあるため、フェノバルビタールを含む医薬品と併用しないでください(4.5を参照)。
てんかん患者の治療を突然中止すると、てんかん重積状態を引き起こす可能性があります。
04.5他の医薬品との相互作用および他の形態の相互作用
関連付けは推奨されません
- エストロゲンとプロゲストゲン(避妊薬として使用):肝臓の異化作用の増加による避妊効果の低下。
避妊の異なる方法、特に機械的な方法を使用することが好ましい。
- アルコール:フェノバルビタールの鎮静作用を増強します。治療中はアルコール飲料やアルコールを含む薬を飲まないでください。
- オトギリソウ:セイヨウオトギリソウベースの製剤を同時に投与すると、フェノバルビタールの有効性が低下する可能性があります。これは、セイヨウオトギリソウベースの製剤による薬物代謝に関与する酵素の誘導によるものであり、フェノバルビタールとの併用投与は避けてください。誘導効果は、セイヨウオトギリソウ製品による治療を停止した後、少なくとも2週間持続する可能性があります。
患者がHypericumperforatum製品を同時に服用している場合は、血中フェノバルビタールレベルを監視し、Hypericumperforatum製品による治療を中止する必要があります。
血中フェノバルビタールレベルは、セイヨウオトギリソウを止めると増加する可能性があります。フェノバルビタールの投与量を調整する必要があるかもしれません。
特別な注意が必要な協会
- シクロスポリン:関連中の活動の減少(異化作用の加速)に伴う循環速度の低下の可能性。逆に、インデューサーの中止後は血漿レベルが上昇します。血漿レベルを制御しながらシクロスポリンの投与量を増やします。インデューサーの中止後は投与量を減らします。
- コルチコイド(グルコ-、ミネラル-、一般的に):コルチコイドの有効性の低下(異化作用の増加)。アディソン人と移植の場合、結果は特に重要です。
臨床的および生物学的防除:関連中および誘導物質の停止後のコルチコイド投与量の適応。
- ドキシサイクリン:ドキシサイクリンの血漿中半減期の減少とその結果としての肝代謝の増加におそらく続発するドキシサイクリンの血漿中濃度の減少。
臨床管理および治療計画の可能な適応(1日量を増やすか、1日2回の投与に分割する)。
- ハイドロキニジン、キニジン:キニジンの血漿レベルの低下と抗不整脈効果(肝代謝の増加)。
臨床管理、ECG、そしておそらくキニジン血症;必要に応じて、インデューサーによる治療中および中止後のキニジンの投与量を調整します(キニジンの過剰摂取のリスク)。
- レボチロキシン:フェニトイン、リファンピシン、カルバマゼピンについて記載されている効果。 T3およびT4の異化作用の増加による甲状腺機能低下症患者の臨床的甲状腺機能低下症のリスク。 T3およびT4の血清レベルを確認し、必要に応じて、インデューサーによる治療中およびその懸濁後にレボチロキシンの投与量を調整します。
- テオフィリン(および外挿により、テオフィリンの誘導体):血漿速度とテオフィリン活性の低下(酵素誘導による代謝の増加)。
臨床および必要に応じてテオフィリンモニタリング。必要に応じて、インデューサーによる治療中およびその懸濁後にテオフィリンの投与量を調整します。
- 葉酸:葉酸投与の場合、活性の低下につながる可能性のある血漿フェノバルビタールレベルの低下(葉酸欠乏のために以前に低下した代謝の正常に戻る)。
おそらく血漿レベルの臨床的管理および必要に応じて、葉酸の投与中およびその懸濁後のフェノバルビタールの投与量の適応。
- バルプロ酸:鎮静(肝異化の阻害)の開始に伴うフェノバルビタールの血漿濃度の増加、子供でより頻繁に。
併用療法の最初の15日間の臨床管理と、鎮静の兆候が現れたときのフェノバルビタール投与量の削減。必要に応じて、フェノバルビタールの血漿レベルを確認してください。
- 経口抗凝固薬:経口抗凝固薬の効果の低下(肝異化作用の増加)。
フェノバルビタールによる治療中および中止後8日間のプロトロンビンレベルのより頻繁なモニタリングおよび経口抗凝固薬投与量の調整。
- イミプラミン抗うつ薬:イミプラミン系抗うつ薬は、全身性発作の発症を助長します。
抗てんかん薬の臨床管理と最終的な投与量の増加。
- ジギトキシン:ジギトキシンの効果の減少(肝臓の異化作用の増加)。
臨床管理、ECG、そしておそらくデジトキシン血症。必要に応じて、併用中およびフェノバルビタール離脱後のジギトキシンの投与量調整;肝臓による代謝が少ないジギトキシンが好ましい。
- Progabide:血漿フェノバルビタールレベルの増加の可能性。血漿プロガビドレベルの低下の可能性があります(検証されていません)。
血漿フェノバルビタールレベルの臨床的およびおそらく制御。ポソロジーの可能な適応。
注意して実装される関連付け
- カルバマゼピン:これが抗てんかん活性に悪影響を与えることなく、血漿カルバマゼピンレベルの漸進的な減少。特に血漿レベルを解釈する際に考慮されるべきである。
- ジソピラミド:ジソピラミドの血漿レベルの低下による抗不整脈効果の低下。
- 他の中枢神経抑制薬:抗うつ薬(A選択的MAOIを除く)、ほとんどの抗H1抗ヒスタミン薬、ベンゾジアゼピン、クロニジンおよびクロニジン様、催眠薬、モルヒネ誘導体(鎮痛薬および抗精神病薬)、神経弛緩薬、ベンゾジアゼピン以外の鎮静剤。
中枢神経抑制の増加。これは、特に運転中または機械の使用時に深刻な結果をもたらす可能性があります。
- フェニトイン:フェノバルビタールとの関連の場合、予測できない変動が発生する可能性があります:フェニトインの血漿レベルは、抗けいれん作用に悪影響を与えることなく、より頻繁に減少します(代謝の増加)。フェノバルビタールが中断されると、フェニトインの毒性作用が現れることがあります。フェニトインの血漿レベルが上昇します(競争による代謝の阻害)。
血漿レベルを解釈する際に考慮されるべきである。
- アルプレノロール、メトプロロール、プロプラノロール(ベータ遮断薬):これらのベータ遮断薬の血漿レベルの低下とその臨床効果の低下(肝代謝の増加)。主に肝臓の生体内変化によって排除されるこれらのベータ遮断薬を考慮に入れること。
04.6妊娠と授乳
妊娠する可能性のある患者または出産可能年齢の患者には、専門家のアドバイスを与える必要があります。
患者が妊娠を計画している場合は、抗てんかん治療の必要性を再評価する必要があります。
先天性欠損症のリスクは、抗てんかん薬で治療された母親の子孫で2〜3倍に増加します。最も頻繁に報告されているのは、口唇裂、心血管奇形、神経管欠損症です。
抗てんかん薬による多剤療法は、単剤療法よりも先天性奇形のリスクが高い可能性があります。したがって、可能な限り単剤療法を実施することが重要です。
発作が再開する危険性があるため、抗てんかん薬治療の突然の中止は、母親と赤ちゃんの両方に深刻な結果をもたらす可能性があるため、実施すべきではありません。
フェノバルビタールで治療された母親の新生児では、出血性症候群が発生する可能性があります。これは、出産の1か月前に母親をビタミンKで治療することで予防できます。フェノバルビタールは胎盤関門を通過し、母乳中に排泄されるため、授乳中にフェノバルビタールを使用することはお勧めしません。
04.7機械の運転および使用能力への影響
フェノバルビタールによる治療は、注意力を低下させ、反射の時間を長くします。患者は、危険性のために車両の運転や警戒の完全性を必要とする活動を行わないように、これについて警告する必要があります。
04.8望ましくない影響
鎮静、運動失調、眼振および精神錯乱は、特に高齢者において、高用量の投与後に発生する可能性があります。まれな皮膚アレルギー症状。
ビタミンK療法に敏感な低プロトロンビン血症は、フェノバルビタールで治療された母親の新生児に発生する可能性があります。慢性治療中に、ビタミンD治療に反応する葉酸感受性巨赤芽球性貧血および骨軟化症が発生する可能性があります。
デュピュイトラン拘縮の症例はめったに報告されていません。
- 皮膚:スティーブンス・ジョンソン症候群(SJS)や中毒性表皮壊死症(TEN)などの重篤な皮膚副作用(SCAR)が報告されています(セクション4.4を参照)。頻度:非常にまれです。多形紅斑のまれな症例が報告されています。
- 肝胆道:毒性肝炎のまれなケース。
- 血液学的:白血球減少症、無顆粒球症、血小板減少症および紫斑病のまれな症例。
- 中枢神経系:一部の被験者では、まれにしか発生しない可能性があります:興奮、興奮、せん妄。多動性の症状は、小児患者で発生する可能性があります。
筋骨格系および結合組織障害
ガーデナーレによる長期治療を受けている患者では、骨塩密度の低下、骨減少症、骨粗鬆症、骨折が報告されています。 Gardenaleが骨代謝に影響を与えるメカニズムは特定されていません。
疑わしい副作用の報告。
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスクバランスを継続的に監視できるため重要です。医療専門家は、国の報告システムを介して疑わしい副作用を報告するよう求められます。 //www.aifa.gov.it/content/segnalazioni-reazioni-avverse。
04.9過剰摂取
過剰摂取後の最初の1時間で、次の症状が現れます:吐き気、嘔吐、頭痛、眠気、精神的混乱、特徴的な自律神経症候群(不規則な緩徐呼吸、気管気管支閉塞、動脈性低血圧)を伴う昏睡状態。急性バルビツール酸中毒の治療は、患者の状態が許せば、即時の胃洗浄を伴います。すでに吸収された薬物の除去は、強制的な利尿と尿のアルカリ化によって達成することができます。重症の場合、血液透析が有用であり、呼吸を機械的に制御する必要があるかもしれません。肺の合併症を避けるために抗生物質の投与が必要です。
05.0薬理学的特性
05.1薬力学的特性
薬物療法グループ:抗てんかん薬、バルビツール酸塩。
ATCコード:N03AA02。
フェノバルビタールは、バルビツール酸塩、抗けいれん薬、催眠鎮静薬です。その活動は、皮質レベルと皮質下レベルの両方で表されます。
05.2薬物動態特性
経口投与されたフェノバルビタールの約80%は消化管から吸収され、血漿ピークは成人では約8時間後、子供では約4時間後に到達します。血漿中半減期は、成人で50〜140時間、小児で40〜70時間です。高齢者や肝不全または腎不全の場合に増加しました。
フェノバルビタールは、その脂溶性のおかげで体全体、特に脳に広がります。それは胎盤の障壁を越え、母乳に排泄されます。
血漿タンパク結合は約50%です。それは肝臓で代謝されて不活性なヒドロキシル化誘導体になり、それが次にグルココンジュゲートまたはスルホン化され、未修飾の形で腎臓を介して排泄されます(尿のアルカリ性が高いほど)。
05.3前臨床安全性データ
06.0医薬品情報
06.1添加剤
トウモロコシ澱粉、ステアリン酸マグネシウム、アルファ化トウモロコシ澱粉。
06.2非互換性
知られていない。
06.3有効期間
36ヶ月
06.4保管に関する特別な注意事項
30°Cを超えない温度で保管してください
06.5即時包装の性質および包装の内容
-ブリスターに50mgの30錠の箱
-ブリスターに100mgの20錠の箱
06.6使用および取り扱いに関する指示
特別な指示はありません。
07.0マーケティング承認保持者
sanofi-aventis S.p.A. --Viale L. Bodio、37 / B-ミラノ
08.0マーケティング承認番号
Gardenale 50mg錠-30錠AICn。 004556027
Gardenale 100mg錠-20錠AICn。 004556015
09.0最初の承認または承認の更新の日付
最初の承認:02.03.1951
承認の更新:2010年6月1日
10.0本文の改訂日
2014年1月













.jpg)