有効成分:タムスロシン(タムスロシン塩酸塩)
Pradif 0.4mg徐放性ハードカプセル
なぜプラディフが使われるのですか?それはなんのためですか?
プラディフの有効成分は、前立腺と尿道の筋肉の緊張を和らげる選択的α1A/α1D拮抗薬であるタムスロシンです。これにより、尿が尿道をより速く通過し、排尿が容易になり、排尿の切迫感が軽減されます。
プラディフは、前立腺肥大症(良性前立腺肥大症)に関連する下部尿路の症状を治療するために男性に使用されます。これらの障害には、尿の通過の困難(ジェットの狭小化)、滴り、緊急性、および排尿の頻度の増加が含まれる場合があります。昼と夜。
Pradifを使用すべきでない場合の禁忌
Pradifを使用しないでください
- タムスロシンまたはプラディフの他の成分のいずれかにアレルギーがある(過敏)場合。過敏症は、身体の軟部組織(喉や舌など)の突然の局所的な腫れ、呼吸困難および/またはかゆみや発疹(血管浮腫)として現れることがあります。
- あなたが深刻な肝臓の問題を抱えているならば、
- 体位を変える(座ったり立ったりする)ときに血圧が下がって失神した場合。
使用上の注意プラディフを服用する前に知っておくべきこと
Pradifには特別な注意を払ってください
- あなたが治療されている状態の進行を監視するために定期的な健康診断が必要です。
- まれに、このタイプの他の薬のようにプラディフを使用すると失神が起こることがあります。めまいや脱力感の最初の兆候が消えるまで、座ったり横になったりする必要があります。
- 重度の腎臓の問題がある場合は、医師に伝えてください。
- 水晶体の曇り(白内障)または眼の圧力上昇(緑内障)のために眼科手術を受けている、または予定されている場合。以前にプラディフを服用したことがあるか、服用している、または服用する予定があるかどうかを眼科医に伝えてください。その結果、専門家は、使用する薬と外科技術に関して最も適切な予防策を講じることができます。水晶体の曇り(白内障)または眼の圧力上昇(緑内障)のために眼科手術を受ける前に、プラディフによる治療を延期または一時的に中止する必要があるかどうかを医師に尋ねてください。
子供達
この薬はこの集団では効果がないため、18歳未満の子供や青年には投与しないでください。
相互作用どの薬や食品がプラディフの効果を変えることができるか
他の薬と一緒にプラディフを服用する
同じクラスに属する他の薬(α1-アドレナリン受容体拮抗薬)と一緒にプラディフを服用すると、血圧が望ましくない低下を引き起こす可能性があります。体からのプラディフ(ケトコナゾール、エリスロマイシンなど)。
処方箋なしで入手した薬を含め、他の薬を服用している、または最近服用したことがあるかどうかを医師または薬剤師に伝えてください。
食べ物や飲み物と一緒にプラディフを取る
プラディフは朝食後またはその日の最初の食事の後に服用する必要があります
警告次のことを知っておくことが重要です。
妊娠、母乳育児、出産
Pradifは女性での使用は適応されていません。
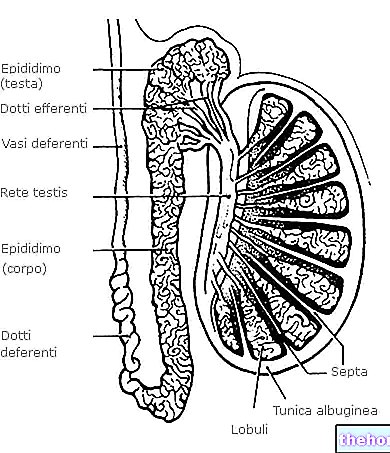
男性では異常な射精(射精障害)が報告されています。これは、精液が尿道を介して体から出ずに膀胱に入る(逆行性射精)か、射精量が減少するか存在しない(射精失敗)ことを意味します。このイベントは無害です。
機械の運転と使用
Pradifは、機械や機器を運転または使用する能力に影響を与えることは示されていません。ただし、めまいが発生する可能性があることを念頭に置いておく必要があります。その場合、注意が必要な活動を行ってはなりません。
投与量、投与方法および投与時間プラディフの使用方法:薬
常に医師の指示どおりにプラディフを服用してください。よくわからない場合は、医師または薬剤師に相談してください。通常の服用量は1日1カプセルで、朝食後またはその日の最初の食事の後に服用します。
カプセルは、つぶしたり噛んだりせずに、丸ごと飲み込む必要があります。
プラディフは通常、長期間処方されます。膀胱と排尿への影響は、プラディフによる長期治療後も維持されます。
過剰摂取プラディフを飲みすぎた場合の対処方法
必要以上にプラディフを服用した場合
プラディフの服用が多すぎると、血圧が低下したり心拍数が上昇したりして、体が弱くなったように感じることがあります。プラディフの服用が多すぎる場合は、すぐに医師に相談してください。
プラディフの服用を忘れた場合
プラディフの服用を忘れた場合は、その日の後半に服用することができます。 1日を逃した場合は、通常の時間にその日のカプセルを服用し続けてください。忘れたものを補うために2回服用しないでください。
Pradifの服用をやめた場合
プラディフ治療を途中で中止すると、初期症状が再発する場合があります。したがって、症状がすでに消えていても、医師の指示がある限り、プラディフを服用し続けてください。この治療を中止すべきだと思われる場合は、必ず医師に相談してください。
この薬の使用についてさらに質問がある場合は、医師または薬剤師に相談してください。
副作用プラディフの副作用は何ですか
すべての薬と同様に、プラディフには副作用がありますが、誰もが副作用を感じるわけではありません。
一般的な影響(10件に1件未満、100件に1件を超える(1〜10%)):
めまい、特に座っているときや立っているとき。
異常な射精(射精障害)。この症状は、精液が尿道を通って体外に出ずに膀胱に入る(逆行性射精)か、精液の量が減少または欠如している(射精障害)ことを意味します。無害です。
まれな影響(1000件に1件以上、100件に1件未満(0.1-1%)):
頭痛、動悸(心臓が通常より頻繁に鼓動し、目立つ)、めまい、鼻づまりまたは鼻水(鼻炎)、下痢、吐き気、嘔吐を伴うことが多い、座ったり横になったりしてすぐに起き上がるなどの血圧の低下、動悸、脱力感(無力症)、皮膚の発赤(発疹)、かゆみ、じんましん。
まれな影響(10,000件に1件以上、1000件に1件未満(0.01-0.1%)):
アレルギー反応(血管浮腫)で頻繁に見られるように、かゆみや皮膚の発赤(発疹)の有無にかかわらず、失神や体の軟部組織(喉や舌など)の突然の局所的な腫れの症例。
非常にまれな影響(10,000件中1件未満(<0.01%)):
持続勃起症(即時の治療を必要とする痛みを伴う長期の非自発的勃起)。発疹、炎症、皮膚および/または唇、目、口、鼻孔または生殖器の粘膜の水疱(スティーブンス・ジョンソン症候群)。
頻度が不明な影響(利用可能なデータから頻度を推定することはできません):
- ぼやけた視界
- 視力障害
- 鼻血(鼻血)
- 重度の皮膚発疹(多形紅斑、剥離性皮膚炎)
- 異常な不規則な心臓リズム(心房細動、不整脈、頻脈)、呼吸困難(呼吸困難)。
- 水晶体の曇り(白内障)または眼圧の上昇(緑内障)のために眼科手術を受けようとしていて、すでにプラディフを服用している、または最近服用した場合、瞳孔の拡張が不十分になり、虹彩(色付きの円形部分)が発生する可能性があります目)手術中にたるむことがあります。
- 口渇。
副作用が深刻になった場合、またはこのリーフレットに記載されていない副作用に気付いた場合は、医師または薬剤師にご相談ください。
副作用の報告
副作用が出た場合は、医師または薬剤師に相談してください。これには、このリーフレットに記載されていない可能性のある副作用も含まれます。 www.agenziafarmaco.gov.it/it/responsabiliの全国報告システムを介して直接副作用を報告することもできます。副作用を報告することにより、この薬の安全性に関する詳細情報を提供するのに役立ちます。
有効期限と保持
元のパッケージで保管してください。
Pradifを子供の手の届かないところに置いてください。
「EXP」(月と年)の後のブリスターとカートンに記載されている有効期限以降は、Pradifを使用しないでください。有効期限は月の最終日を指します。
薬は廃水や家庭ごみとして処分しないでください。使用しなくなった薬は薬剤師に捨ててください。環境保護に役立ちます。
組成および剤形
Pradifに含まれるもの
有効成分は塩酸タムスロシンです。
その他の成分は次のとおりです。カプセルの内容:微結晶性セルロース(E460)。メタクリル酸-アクリル酸エチル共重合体(1:1);ポリソルベート80(E433);ラウリル硫酸ナトリウム;トリアセチン(E1518);ステアリン酸カルシウム(E470a);タルク(E553b)。カプセルシェル:ハードゼラチン;インジゴカルミン(E132);二酸化チタン(E171);黄色の酸化鉄(E172);赤い酸化鉄(E172)。印刷インキ:シェラック(E904)、プロピレングリコール(E1520)、黒色酸化鉄(E172)。
Pradifの外観とパックの内容の説明
プラディフカプセルはオレンジ/オリーブグリーンで、T0.4コードとロゴが付いています。
プラディフカプセルは、段ボール箱に入ったポリプロピレン-アルミニウムブリスターにパッケージされています。
パックには、10、20、30、50、60、90、100、または200カプセルが含まれています。すべてのパックサイズが販売されているわけではありません
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
プラディフハードカプセル
02.0定性的および定量的組成
各徐放性カプセルには、有効成分として0.4mgの塩酸タムスロシンが含まれています。
添加剤:添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形
オレンジ/オリーブグリーンの徐放性カプセル、ハード、T0.4コードとロゴが付いています。
04.0臨床情報
04.1治療適応
良性前立腺肥大症(BPH)に関連する下部尿路症状(LUTS)。
04.2投与の形態と方法
経口使用。
朝食後またはその日の最初の食事の後に服用する1日1カプセル。
カプセルは丸ごと飲み込む必要があり、有効成分の徐放性を妨げる可能性があるため、押しつぶしたり噛んだりしないでください。
腎機能障害の場合、投与量の調整は必要ありません。
軽度から中等度の肝不全の場合、投与量の調整は必要ありません(セクション4.3禁忌も参照)。
小児人口
小児におけるプラディフの特定の使用についての兆候はありません。
小児におけるタムスロシンの安全性と有効性
04.3禁忌
薬物誘発性血管浮腫を含む塩酸タムスロシンまたはいずれかの賦形剤に対する過敏症;起立性低血圧の病歴;重度の肝不全。
04.4使用に関する特別な警告と適切な注意事項
他のa1-アドレナリン受容体拮抗薬と同様に、プラディフによる治療中に、特定の場合に血圧の低下が起こることがあり、まれに失神につながる可能性があります。起立性低血圧の最初の兆候(めまい、脱力感)では、症状が消えるまで患者は座るか横になる必要があります。
プラディフ療法を開始する前に、良性の前立腺肥大症と同じ症状を引き起こす可能性のある他の状態について患者を評価する必要があります。直腸検査および必要に応じて前立腺特異抗原(PSA)の測定は、治療を開始する前とその後定期的に実施する必要があります。
重度の腎機能障害(クレアチニンクリアランスが10ml /分未満)の患者の治療は、これらの被験者で医薬品が研究されていないため、注意して検討する必要があります。
術中虹彩緊張症候群(IFIS、小瞳孔症候群の変種)は、塩酸タムスロシンを服用している、または以前に治療した一部の患者の白内障および緑内障手術中に観察されています。
IFISは、手術中および手術後の眼の合併症のリスクを高める可能性があります。
白内障または緑内障手術の1〜2週間前に塩酸タムスロシンを中止することは経験的に有用であると考えられていますが、治療を中止することの利点はまだ確立されていません。
IFISは、手術前にタムスロシンを長期間中止した患者にも見られます。
白内障または緑内障の手術が計画されている患者に塩酸タムスロシンによる治療を開始することは推奨されません。
術前評価の際、眼科医と外科チームは、白内障または緑内障の手術を待っている患者が治療中であるか、タムスロシンで治療されているかを検討して、介入中にIFISを管理するための適切な措置を講じることができるようにする必要があります。
タムスロシン塩酸塩は、CYP2D6表現型の代謝が不十分な患者にCYP3A4の強力な阻害剤と組み合わせて投与すべきではありません。
タムスロシン塩酸塩は、CYP3A4の強力および中程度の阻害剤と組み合わせて注意して使用する必要があります(セクション4.5を参照)。
04.5他の医薬品との相互作用および他の形態の相互作用
相互作用の研究は成人でのみ実施されています。
塩酸タムスロシンをアテノロール、エナラプリル、またはテオフィリンと併用した場合、相互作用は認められませんでした。
シメチジンを併用すると、血漿タムスロシンレベルが上昇し、フロセミドはそれらを低下させます。ただし、タムスロシンの血漿中濃度レベルは治療範囲内であるため、投与量の調整は必要ありません。
試験管内で ジアゼパム、プロプラノロール、トリクロルメチアジド、クロルマジノン、アミトリプチリン、ジクロフェナク、グリベンクラミド、シンバスタチン、およびワルファリンは、ヒト血漿中のタムスロシンの遊離画分を変化させません。タムスロシンは、ジアゼパム、プロプラノロール、トリクロルメチアジド、およびクロルマジノンの遊離画分を修飾しません。
ただし、ジクロフェナクとワルファリンはタムスロシンの排泄率を高める可能性があります。
タムスロシン塩酸塩と強力なCYP3A4阻害剤の併用投与は、タムスロシン塩酸塩への曝露の増加につながる可能性があります。ケトコナゾール(CYP3A4の既知の強力な阻害剤)との併用投与は、タムスロシン塩酸塩のAUCおよびCmaxをそれぞれ2.8倍および2.2倍増加させました。
タムスロシン塩酸塩は、CYP2D6表現型の代謝が不十分な患者にCYP3A4の強力な阻害剤と組み合わせて投与すべきではありません。
タムスロシン塩酸塩は、CYP3A4の強力および中程度の阻害剤と組み合わせて注意して使用する必要があります。
塩酸タムスロシンとCYP2D6の強力な阻害剤であるパロキセチンの同時投与により、タムスロシンのCmaxとAUCがそれぞれ1.3倍と1.6倍に増加しましたが、これらの増加は臨床的に関連があるとは見なされていません。
他のa1-アドレナリン受容体拮抗薬を併用すると、血圧降下作用を引き起こす可能性があります。
04.6妊娠と授乳
Pradifは女性での使用は適応されていません。
塩酸タムスロシンを用いた短期および長期の臨床試験で射精障害が観察されています。射精障害、逆行性射精、射精不能の症例が認可後の研究で報告されています。
04.7機械の運転および使用能力への影響
機械を運転して使用する能力に関する研究は行われていませんが、患者はめまいの可能性に注意する必要があります。
04.8望ましくない影響
*市販後調査で観察
タムスロシン療法に関連する「術中虹彩緊張症候群」(IFIS)として知られる小瞳孔症候群の変種が、市販後調査期間中の白内障および緑内障手術中に観察されています(セクション4.4も参照)。
市販後の経験:上記の有害事象に加えて、タムスロシンの使用に関連して心房細動、不整脈、頻脈、呼吸困難が報告されています。これらの自発的に報告された事象は、世界中での市販後の経験に由来するため、頻度とそれらを引き起こすことにおけるタムスロシンの役割は確実に決定することができません。
疑わしい副作用の報告
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスクバランスを継続的に監視できるため重要です。医療専門家は、国の報告システムを介して疑わしい副作用を報告するよう求められます。 agenziafarmaco.gov.it/it/responsabili。
04.9過剰摂取
症状
塩酸タムスロシンの過剰摂取は、重度の血圧降下作用を引き起こす可能性があります。
重度の降圧効果は、さまざまなレベルの過剰摂取で観察されました。
処理
過剰摂取後の急性低血圧の場合は、心血管系をサポートするために迅速な行動を取る必要があります。
患者さんを寝かせることで、血圧と心拍数を正常に戻すことができます。
これが十分でない場合は、増量剤と、必要に応じて血管収縮薬を使用できます。腎機能を監視し、一般的な支援策を適用する必要があります。
タムスロシンは血漿タンパク質に強く結合するため、透析はほとんど役に立ちません。吸収を防ぐために、嘔吐などのいくつかの対策を講じることができます。
大量摂取の場合、胃洗浄が有用であり、活性炭および硫酸ナトリウムなどの浸透圧性緩下薬を投与することができます。
05.0薬理学的特性
05.1薬力学的特性
薬物療法グループ:a1アドレナリン受容体拮抗薬。
ATCコード:G04CA02。
前立腺病変の排他的治療のための準備。
作用機序:
タムスロシンは、シナプス後のa1アドレナリン受容体、特にa1Aおよびa1Dサブタイプに選択的かつ競合的に結合します。前立腺と尿道の平滑筋を弛緩させます。
薬力学的効果:
プラディフは最大尿流を増加させます。前立腺と尿道の平滑筋を弛緩させることで閉塞を緩和し、それによって排尿症状を改善します。
また、膀胱の不安定性が重要な役割を果たす充填症状を改善します。
症状の充満と排出に対するこれらの影響は、長期治療中も維持されます。手術やカテーテル挿入の必要性は大幅に遅れています。
A1-アドレナリン受容体拮抗薬は、末梢抵抗を低下させることによって血圧を低下させることができます。 Pradifを使用した臨床試験では、臨床的に有意な血圧の低下は観察されませんでした。
小児人口
神経因性膀胱の小児を対象に、二重盲検、ランダム化、プラセボ対照、用量設定試験が実施されました。合計161人の子供(2〜16歳)が無作為化され、タムスロシンの3つの用量レベル(低[0.001〜0.002 mg / kg]、中[0.002〜0.004 mg / kg]、高[0.004〜0.004 mg / kg])の1つで治療されました。 0.008 mg / kg])、またはプラセボを使用。主要評価項目は、消失点排尿筋圧(排尿筋のリークポイント圧力、LPP)は、水腎症と水尿管が安定し、カテーテル挿入日誌に記録されているように、カテーテル挿入から得られた尿量とカテーテル挿入中の尿漏れの数が変化するまで減少しました。一次エンドポイントまたは二次エンドポイントのいずれについても、プラセボ群と3つのタムスロシン群のいずれにも有意差はありませんでした。どの用量レベルでも用量反応は観察されませんでした。
05.2薬物動態特性
吸収
タムスロシン塩酸塩は腸から吸収され、ほぼ完全に生物学的に利用可能です。
タムスロシン塩酸塩の吸収は、食事に近づけることで減少します。
患者が常に同じ食事の後にプラディフを服用すれば、均一な吸収を達成することができます。
タムスロシンは線形速度論を示します。
摂食状態でのプラディフの単回投与後、タムスロシンの血漿レベルは約6時間でピークに達し、5日間の治療後に到達する定常状態条件下では、Cmaxは単回投与後の達成値よりも約2/3高くなります。
これは高齢の患者で指摘されており、若い患者でも同じことを期待するのは合理的です。
単回投与と反復投与の両方の後、血漿レベルにはかなりの個人差があります。
分布
ヒトでは、タムスロシンは血漿タンパク質に約99%結合しています。分布容積は小さいです(約0.2 l / kg)。
生体内変化
タムスロシンは代謝が遅いため、初回通過効果が不十分です。
タムスロシンは、主に未変化の有効成分の形で血漿中に存在します。
肝臓で代謝されます。
タムスロシンによって引き起こされるミクロソーム肝酵素系の誘導は、ラットでは事実上観察されなかった。
インビトロの結果は、CYP3A4およびCYP2D6も代謝に関与しており、他のCYPアイソザイムによる塩酸タムスロシンの代謝にわずかに寄与している可能性があることを示唆しています。薬物代謝酵素CYP3A4およびCYP2D6の阻害は、塩酸タムスロシンへの曝露の増加につながる可能性があります(セクション4.4および4.5を参照)。
元の製品よりも活性の高い代謝物はありません。
排除
タムスロシンとその代謝物は主に尿から排出され、投与量の約9%が未変化の活性物質の形で排出されます。
摂食状態および定常状態でのプラディフの単回投与後、排泄半減期はそれぞれ10時間および13時間で評価されました。
05.3前臨床安全性データ
マウス、ラット、イヌで単回および反復投与毒性試験を実施した。ラットでの生殖試験、マウスとラットでの発がん性試験、遺伝子毒性試験も検討された。 インビボ と 試験管内で.
高用量のタムスロシンで確認された一般的な毒物学的プロファイルは、a1アドレナリン受容体拮抗薬の既知の薬理学的活性と一致しています。
犬では、非常に高用量で心電図が変化します。この反応は臨床的に関連性がないと見なされます。
タムスロシンは、関連する遺伝子毒性を示さなかった。
「ラットおよび雌マウスの乳房における増殖性変化の発生率の増加が報告されている。これらの所見は、高プロラクチン血症によって媒介される可能性が高く、高用量でのみ発生するが、無関係と見なされる」。
06.0医薬品情報
06.1添加剤
カプセルの内容:
微結晶性セルロースE460、メタクリル酸-アクリル酸エチルコポリマー(1:1)、ポリソルベート80 E433、ラウリル硫酸ナトリウム、トリアセチンE1518、ステアリン酸カルシウムE470a、タルクE553b。
カプセル:
ハードゼラチン、インディゴカーマインE132、二酸化チタンE171、黄色酸化鉄E172、赤色酸化鉄E172。
印刷インキ:
シェラックE904、プロピレングリコールE1520、黒色酸化鉄E172。
06.2非互換性
関係ありません。
06.3有効期間
4年。
06.4保管に関する特別な注意事項
元のパッケージで保管してください。
06.5即時包装の性質および包装の内容
ポリプロピレン-10カプセルのアルミニウムブリスター、10、20、30、50、60、90、100、200カプセルのカートン。
PVC / PVDC-5カプセルのアルミニウムブリスター、50カプセルの箱に入っています。
すべてのパックサイズが販売されているわけではありません。
06.6使用および取り扱いに関する指示
特別な指示はありません。
07.0マーケティング承認保持者
Boehringer Ingelheim International GmbH-Binger Strasse 173-D 55216 Ingelheim amRhein-ドイツ
イタリア代表
ベーリンガーインゲルハイムイタリアS.p.A. --Via Lorenzini、8-20139ミラノ
08.0マーケティング承認番号
20カプセルの箱:A.I.C。 N°030106013
30カプセルのパック:A.I.C。 N°030106025
09.0最初の承認または承認の更新の日付
1996年9月27日/ 2006年7月12日。
10.0本文の改訂日
10.06.2014.