シスプラチンは、次のクラスに属する化学療法薬です。 アルキル化剤。それは強力な抗腫瘍剤と考えられているので、世界保健機関によって作成された必須医薬品のリストに含まれています。

治療上の適応症
シスプラチンは、以下を含むさまざまな種類の癌の治療のために、単独で、または他の抗癌剤と組み合わせて使用することができます。
- 進行性または転移性の卵巣癌;
- 進行性または転移性の膀胱がん;
- 精巣癌、進行性または転移性;
- 進行性または転移性の小細胞および非小細胞肺がん
- 頭頸部の扁平上皮がん、進行性および転移性。
シスプラチンは精巣癌の治療に特に効果的です:と組み合わせて使用した場合 ブレオマイシン (細胞毒性抗生物質)または ビンブラスチン (有糸分裂阻害剤)は回復の可能性を大幅に高めます。
シスプラチンは、と組み合わせて使用することもできます オージェ療法、特定のタイプの 放射線療法 これは、低エネルギー電子ビームを使用して、腫瘍を構成する悪性細胞を照射します。
実施された研究と臨床効果
1.進行性非小細胞肺癌の治療におけるシスプラチンとの併用療法
Zhongliu Yaoxue、3、293-296
進行した非小細胞肺癌の治療における、それぞれシスプラチンと組み合わせたペメトレキセドおよびドセタキセルの臨床的有効性に関する観察
馬、清;張、Junfeng; Li、Jianjun; Bai、Qinxia;劉、ヤンタン
シスプラチンは、他の抗がん剤と組み合わせて使用されることがよくあります。
この研究は、ペメトレキセド、ドセタキセル、シスプラチンとの併用療法の有効性と安全性を確立するために実施されました。
進行した非小細胞肺癌の97人の患者に実施されました。患者は2つのグループに分けられました。 1つのグループはと組み合わせてシスプラチンを与えられました ペメトレキセド (エージェント 代謝拮抗剤)、他のグループはシスプラチンと組み合わせて与えられました ドセタキセル (エージェント 有糸分裂阻害剤).
この研究は、2つの治療戦略が同じ有効性を持っていることを示しました。しかし、ペメトレキセドおよびシスプラチン療法は、ドセタキセル療法よりも、白血球減少症、貧血、血小板減少症、悪心および嘔吐などの副作用の発生率が有意に低いことを示しました。
2.進行胃癌の治療におけるシスプラチン、フルオロウラシルおよびエレミエマルジョンとの併用療法
Zhongguo Yaoye、23、53-55
64例の進行胃癌の治療におけるシスプラチンとフルオロウラシルを組み合わせたエレミ経口エマルジョンの臨床評価
さあ、Xiaohui
L」エレミ の家族に属する植物の幹を切断することによって得られるオレオレジンです カンラン科.
この研究では、進行胃癌に苦しむ64人の患者がシスプラチンとフルオロウラシルに基づく併用療法を受け、それに「エレミエマルジョン」の経口投与が追加されました。この研究は、薬物とエマルジョンの組み合わせが副作用を増加させることなく治療。実際、シスプラチンとフルオロウラシルのみの治療では、1年生存率は45%であることがわかりました。しかし、エマルジョンを加えると、生存率は56%に増加するようです。
3.ベチバーオイル摂取後のシスプラチンによる副作用の緩和
食品および化学毒性学、81、120-128
ベチバーオイル(Java)は、スイスアルビノマウスのシスプラチン誘発性の酸化ストレス、腎毒性、骨髄抑制を軽減します
シンハ、ソナリ; Jothiramajayam、マニヴァンナン; Ghosh、Manosij;ヤナ、アディティ;チャッテルジ、ウルミ; Mukherjee、Anita
シスプラチンの使用は、その有効性にもかかわらず、それに伴う重い副作用のために制限されています。
この研究の目的は、「ジャワベチバーオイル。評価は、シスプラチン投与前の7日間、経口ベチバーオイルを投与されたスイスアルビノマウスで実施されました。この期間の後、薬が投与されました。この研究は、シスプラチンによって誘発される腎毒性と骨髄抑制の有意な減弱を示しました。したがって、この研究は、シスプラチン療法によって誘発される副作用に対するベチバーオイルの興味深い保護能力を強調しています。
警告
シスプラチンは、抗がん化学療法剤の投与を専門とする医師の厳密な監督下で投与する必要があります。
薬剤は感光性であるため、暗いボトルに梱包されています。したがって、光を避けて保管する必要があります。
シスプラチンは金属アルミニウムと反応して黒色の白金沈殿物を形成するため、アルミニウムを含む針、注射器、カテーテルの使用を避けて薬剤を投与する必要があります。
治療期間全体の前、最中、後は、 監視 NS 腎臓機能, 苔類, 造血 (血球の量)と 血清電解質 (カルシウム、マグネシウム、ナトリウム、カリウム)。
相互作用
他の物質と併用したシスプラチンの投与 腎毒性 (すなわち、腎臓に毒性がある)-例えば、セファロスポリン、アミノグリコシドまたは造影剤など-は腎臓への毒性効果を増強します。
シスプラチンによる治療中および治療後は、主に腎臓から排泄される他の薬剤を注意して使用することをお勧めします。
薬物の同時投与 耳毒性 (耳に有毒)-アミノグリコシドやループ利尿薬など-は、耳へのシスプラチンの毒性を強める可能性があります。
L」イホスファミド (NS 抗腫瘍アルキル化剤)シスプラチンによる治療による難聴のリスクを高める可能性があります。
の現代的な使用 骨髄抑制剤 または 放射線療法 それらはシスプラチンの骨髄抑制活性を高めることができます。
シスプラチンを組み合わせて投与する場合 ビンブラスチン また ブレオマイシン レイノー現象を引き起こす可能性があります。
シスプラチンeの併用投与 ドセタキセル 誘発することができます 神経毒性作用 (神経系に有毒)2つの薬の単回摂取によって誘発されるものよりも深刻です。
シスプラチンの有効性は、いくつか服用することで低下する可能性があります キレート剤、たとえば、 ペニシラミン.
副作用
シスプラチンの投与による副作用は、投与量によって、また薬剤が単剤療法と併用化学療法のどちらで使用されるかによって異なります。さらに、ある個人と別の個人の間でさえ、応答には大きなばらつきがあります。
以下は、シスプラチン治療の副作用の一部です。
腎毒性
シスプラチンは 非常に腎毒性 (腎臓に有毒)、特に既存の腎機能障害のある患者では。シスプラチンの腎毒性は 用量制限の副作用:このタイプの毒性は、患者に投与できる薬剤の投与量を減らすことを意味します。
神経毒性
三 神経毒性 シスプラチンによって引き起こされる 用量依存つまり、服用する薬の投与量が増えると増加します。 知覚異常 (手足または体の他の領域の感覚の喪失)、 反射低下 (反射神経の完全な喪失)および 固有受容感覚の喪失つまり、空間内での自分の体の位置を認識および認識する能力の喪失です。
シスプラチン治療中および治療後に定期的な神経学的検査を実施する必要があります。
聴器毒性
それは通常、次の形で現れます 耳鳴り (口笛、ブーンという音、ざわめく、または耳の中でズキズキする)および/または 難聴。難聴は片側性または両側性であり、繰り返し投与するとより重篤になる傾向があります。この副作用を防ぐ効果的な治療法はありません。これは、大人よりも子供に顕著である可能性があります。
シスプラチン療法を開始する前および投与の合間に、注意深い聴力検査を実施する必要があります。
骨髄抑制
シスプラチンは誘発することができます 骨髄抑制、それは 骨髄抑制。この削除により、 造血の減少 (血球の合成の減少)。
血球合成の低下は、以下につながる可能性があります。
- 貧血 (血中のヘモグロビンの量の減少);
- 白血球減少症 (白血球数の減少)結果として 感染症にかかりやすくなります;
- 血小板減少症 (血小板数の減少) 出血のリスクが高まります。
骨髄抑制は副作用です 用量依存.
吐き気と嘔吐
シスプラチンは強力なものです 催吐性 (嘔吐を誘発します)そして-制吐(抗嘔吐)薬が投与されない限り-この副作用はほとんど常に起こります。
一般的に、制吐剤(例えば、 オンダンセントロン)コルチコステロイドとの組み合わせ(例えば、 デキサメタゾン).
電解質の乱れ
シスプラチンは原因となる可能性があります 低マグネシウム血症, 低カリウム血症 と 低カルシウム血症、または-それぞれ-血中のマグネシウム、カリウム、カルシウムのレベルの低下。
心臓の病状
シスプラチン療法は誘発することができます 心不整脈、含まれています 徐脈 と 頻脈。特に、これらの効果は、シスプラチンを他の細胞毒性薬と組み合わせて使用した場合に観察されています。
それは現れることができます 高血圧 そして、場合によっては、それが発生する可能性があります 心筋梗塞 治療終了後数年でも。
血管の病状
それが発生することは非常に一般的です 静脈炎 シスプラチンが注射される領域で。
それらはまた発生する可能性があります 脳虚血 また 心筋.
呼吸器の病状
それらはシスプラチンによる治療後に発生する可能性があります 呼吸困難, 呼吸不全 そして、場合によっては、 肺炎.
肝胆道障害
シスプラチンは、肝機能障害と血中濃度の上昇を引き起こす可能性があります トランスアミナーゼ (肝臓の損傷の可能性を検出するための指標として使用される酵素)および ビリルビン (胆汁に含まれる黄色の色素、ヘモグロビンの異化作用によって生成されます)。
皮膚および皮下組織の障害
彼らは現れることができます 紅斑, 潰瘍 と 皮膚の発疹 シスプラチンが注射された領域で。また、それが発生する可能性があります 脱毛症.
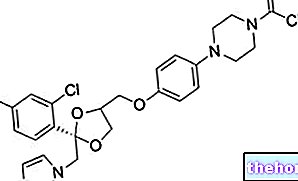
作用機序
シスプラチンは、すべてのアルキル化剤と同様に、DNAを構成する2本の鎖と結合を形成することができます。

DNAは、二重らせんを形成するために互いに結合された2本の鎖で構成されています。
DNAはヌクレオチドと呼ばれる多くのモノマーで構成されています。ヌクレオチドには、アデニン(A)、グアニン(G)、シトシン(C)、チミン(T)の4種類があり、水素結合によって結合された固有のAT(アデニン-チミン)とCG(シトシン-グアニン)のペアと結合します。 。
DNA分子に沿って存在する塩基の配列は遺伝情報を運びます。
DNAの二本鎖はと呼ばれる4つの基本単位で構成されています 窒素塩基:これらの分子は、シトシン、チミン、アデニン、グアニンです。シスプラチンは、グアニンの構造に存在する窒素原子に結合することで細胞毒性作用を発揮しますが、アデニンとの結合を形成することもできます。シスプラチンがDNA鎖に結合すると、これが転写および複製されるのを防ぎ、細胞がメカニズムを満たすことを非難します。の プログラム細胞死 (アポトーシス).
使用方法-投与量
シスプラチンは透明で淡黄色の液体です。管理は通常のために行われます 静脈内注入 6〜8時間以内。
投与されるシスプラチンの用量は、治療しようとしている癌の種類と、その薬を単独で使用するか、他の薬と組み合わせて使用するかによって異なります。
単剤療法
シスプラチン単独では、2つの異なる方法で投与できます。
- 単回投与、3〜4週間ごとに体表面の50〜120mg / m2の範囲の量;
- 分割線量、1日あたり15〜20 mg / m2の範囲の量で、3〜4週間ごとに5日間連続して。
これらの用量は、大人と子供の両方に投与することができます。
併用化学療法
シスプラチンを併用化学療法で使用する場合は、投与量を減らす必要があります。通常、通常の投与量は20 mg / m2以上で、3〜4週間ごとに1回投与します。
子宮頸がんの治療の場合、シスプラチンは通常、放射線療法と組み合わせて使用されます。この場合、通常の投与量は、週に40 mg / m2、6週間です。
シスプラチンの腎毒性のため、腎機能障害のある患者では投与量を減らす必要があります。
シスプラチンによって引き起こされる腎臓の損傷を回避するか、少なくとも封じ込めるために、患者は塩化物を含む溶液で水分補給する必要があります。それらは投与することができます 生理食塩水利尿薬 また マンニトール 治療中および治療後の継続的な薬物排泄を促進するため。
妊娠と母乳育児
妊婦によるシスプラチンの使用に関するデータは不十分ですが、深刻な先天性欠損症を引き起こす可能性があると考えられています。
しかし、動物で行われた研究は、 生殖毒性 と 経胎盤発がん性。したがって、シスプラチンは妊娠中の女性に投与すると胎児に有毒である可能性があるため、使用を避けることを強くお勧めします。
妊娠を避けるために、シスプラチン療法中および治療後少なくとも6か月間は、男女ともに予防措置を講じる必要があります。
シスプラチンは母乳にも排泄されるため、授乳中の使用はお勧めしません。
禁忌
シスプラチンの使用は、薬物自体または他のプラチナ含有化合物にアレルギーのある患者には禁忌です。
シスプラチンは、骨髄抑制のある患者、腎機能障害のある患者、および脱水状態の患者には禁忌です。また、聴覚障害のある患者には禁忌です。
シスプラチンの発見
化学と医学の世界に革命をもたらした多くの発見のように、シスプラチンの細胞毒性作用の発見も偶然に起こりました。
もともと、シスプラチンは1845年にイタリアの化学者ミケーレペイロンによって最初に記述され、長い間「塩化ペイロン」として知られていました。

実験はの細菌培養で実施されました 大腸菌 2つの白金電極を含むチャンバー内で塩化アンモニウム(細菌の増殖に必要)を含む培地で培養。
科学者たちは、電界が印加されると、細菌の複製が停止したことに注目しました。バクテリアの成長は中断されませんでしたが、それらはもはや正常な方法ではなく、異常な方法で成長しました。科学者たちは、電場を適用すると、細菌の増殖を変化させ、それらの複製を阻止することができる化学種が生成されたと推測しました。ローゼンバーグの研究は、細胞毒性作用が有機金属錯体の形成によるものであると理解するまで続けられました。 シスプラチン.
その後、癌の治療におけるシスプラチンの可能性を評価するために多くの研究が行われました。
1978年12月、米国食品医薬品局は精巣癌および卵巣癌の治療にシスプラチンを使用することを承認し、翌年には他のヨーロッパ諸国で承認されました。