有効成分:メトクロプラミド
プラシル10mg錠
Plasilの添付文書はパックで利用できます:- プラシル10mg錠
- プラシル10mg / 10mlシロップ
- PLASIL 10 mg / 2ml注射用溶液
なぜプラシルが使われるのですか?それはなんのためですか?
プラシルは胃腸機能障害の薬のクラスに属し、強力な制吐特性を腸の運動促進活性と関連付けます。
治療上の適応症
成人人口
プラシルは成人に次のように適応されます:
- 化学療法誘発性悪心および嘔吐(CINV)の遅延の予防
- 放射線療法誘発性の悪心および嘔吐(RINV)の予防
- 急性片頭痛誘発性の悪心および嘔吐を含む、悪心および嘔吐の対症療法。メトクロプラミドは、急性片頭痛における鎮痛薬の吸収を改善するために経口鎮痛薬と組み合わせて使用することができます。
小児人口
プラシルは、1〜18歳の子供に次の理由で適応されます。
- セカンドラインオプションとしての遅延化学療法誘発性悪心および嘔吐(CINV)の予防
Plasilを使用すべきでない場合の禁忌
- 活性物質またはセクション6.1に記載されている賦形剤のいずれかに対する過敏症
- 胃腸の運動性の刺激がリスクをもたらす胃腸出血、機械的閉塞または胃腸穿孔
- 重度の高血圧のエピソードのリスクによる褐色細胞腫の確認または疑い
- 緑内障の患者
- 神経弛緩薬またはメトクロプラミドによって誘発された遅発性ジスキネジーの病歴
- てんかん(発作の頻度と強度の増加)
- パーキンソン病
- レボドパまたはドーパミン作動薬との併用(「相互作用」のセクションを参照)
- メトクロプラミドを伴うメトヘモグロビン血症またはNADHチトクロームb5レダクターゼ欠損症の既知の病歴
- 錐体外路障害のリスクが高いため、1歳未満の子供に使用します(「特別な警告」のセクションを参照)。
使用上の注意Plasilを服用する前に知っておくべきこと
腎不全および肝不全
腎不全または重度の肝不全の患者では、投与量を減らすことをお勧めします(「投与量、投与方法および投与時間」のセクションを参照)。
心臓の病状
循環虚脱、重度の徐脈、心停止、QT間隔の延長など、深刻な心血管系の望ましくない影響が、特に静脈内に注射可能なメトクロプラミドを投与した後に報告されています(「望ましくない影響」のセクションを参照)。
メトクロプラミドを、特に高齢者、心臓伝導障害(QT間隔の延長を含む)の患者、電解質の不均衡、徐脈が矯正されていない患者、およびQT間隔を延長することが知られている他の薬剤を服用している患者に静脈内投与する場合は特に注意が必要です。
静脈内投与は、副作用(例えば、低血圧、アカシジア)のリスクを減らすために、ゆっくりとしたボーラス(少なくとも3分間の持続時間)として与えられるべきです。
特に乳がんまたはプロラクチン分泌性下垂体腺腫の患者では、プロラクチンレベルの上昇の可能性を慎重に検討する必要があります。
メトクロプラミドとアルコール飲料の併用はお勧めしません。
相互作用どの薬や食品がプラシルの効果を変えることができるか
最近、処方箋のない薬でも、他の薬を服用したことがある場合は、医師または薬剤師に伝えてください。
禁忌の関連
レボドパまたはドーパミン作動薬とメトクロプラミドは互いに拮抗します(「禁忌」のセクションを参照)。
避けるべき関連:
アルコールはメトクロプラミドの鎮静効果を高めます
考慮すべき関連:
メトクロプラミドの運動促進効果により、一部の薬物の吸収が損なわれる可能性があります。
抗コリン作用薬およびモルヒネ誘導体
抗コリン作用薬とモルヒネ誘導体は両方とも、消化管の運動性に対してメトクロプラミドに対して拮抗作用を示す可能性があります。
中枢神経系抑制剤(モルヒネ誘導体、抗不安薬、鎮静H1抗ヒスタミン薬、鎮静抗うつ薬、バルビツール酸塩、クロニジンおよび関連薬)
CNS抑制薬とメトクロプラミドの鎮静効果が増強されます。
神経弛緩薬
メトクロプラミドは、錐体外路障害の場合、他の神経弛緩薬と相加効果がある可能性があります。
セロトニン作動薬
SSRIなどのセロトニン作動薬と一緒にメトクロプラミドを使用すると、セロトニン症候群のリスクが高まる可能性があります。
ジゴキシン
メトクロプラミドは、ジゴキシンの生物学的利用能を低下させる可能性があります。ジゴキシンの血漿中濃度を綿密に監視する必要があります。
シクロスポリン
メトクロプラミドはシクロスポリンの生物学的利用能を増加させます(Cmaxは46%、曝露は22%)。シクロスポリン血漿濃度の綿密なモニタリングが必要です。臨床的影響は不確実です。
ミバクリウムとスキサメトニウム
メトクロプラミドの注射は、神経筋遮断の期間を延長することができます(血漿コリンエステラーゼの阻害を通じて)。
CYP2D6の強力な阻害剤
フルオキセチンやパロキセチンなどの強力なCYP2D6阻害剤と併用すると、メトクロプラミドの曝露レベルが上昇します。臨床的意義は不明ですが、患者は副作用がないか監視する必要があります。
シスプラチン
いくつかの観察は、メトクロプラミドで、シスプラチンの腎毒性の増加を報告しています。
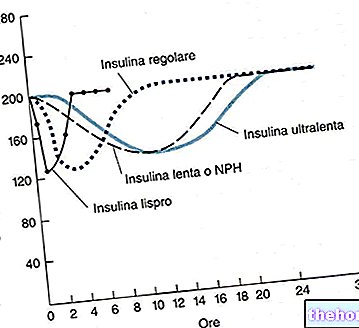
インスリン
メトクロプラミド治療は、食物を含む腸管通過を減らすことにより、糖尿病におけるインスリン投与量の調整を必要とする場合があります。メトクロプラミドはまた、S.N.C。に対するアポモルヒネの影響を軽減します。
警告次のことを知っておくことが重要です。
神経学的障害
錐体外路障害は、特に子供や若年成人、および/または高用量の使用で発生する可能性があります。これらの反応は通常、治療の開始時に発生し、単回投与後に発生する可能性があります。錐体外路症状の場合は、メトクロプラミドを直ちに中止する必要があります。これらの効果は通常、治療の中止後に完全に可逆的ですが、対症療法が必要になる場合があります(小児ではベンゾジアゼピン、成人では抗コリン作用薬および抗パーキンソン薬)。過剰摂取の場合を避けるために、「投与量、投与方法および投与時間」の段落で指定されているように、2回の投与の間の少なくとも6時間の時間間隔は、嘔吐および投与の拒絶の場合でも尊重されなければならない。
メトクロプラミドによる長期治療は、特に高齢者において、潜在的に不可逆的な遅発性ジスキネジーを引き起こす可能性があります。遅発性ジスキネジアのリスクがあるため、治療期間は3か月を超えてはなりません(「望ましくない影響」のセクションを参照)。遅発性ジスキネジーの症状が現れた場合は、治療を中止する必要があります。
神経遮断薬悪性症候群は、メトクロプラミドと神経弛緩薬の併用、およびメトクロプラミドによる単剤療法で報告されています(「望ましくない影響」のセクションを参照)。神経遮断薬の悪性症候群の症状が発生した場合は、メトクロプラミドを直ちに中止し、適切な治療を開始する必要があります。神経疾患を併発している患者、および中枢神経系に作用する他の薬剤で治療されている患者には、特に注意を払う必要があります(「禁忌」のセクションを参照)。
パーキンソン病の症状は、メトクロプラミドによって悪化する可能性があります。
メトヘモグロビン血症
NADHチトクロームb5レダクターゼ欠損症に関連している可能性のあるメトヘモグロビン血症が報告されています。そのような場合、メトクロプラミドは直ちにそして永久に中止されるべきであり、適切な措置(メチレンブルー治療など)が取られるべきです。
妊娠と母乳育児
薬を服用する前に、医師または薬剤師にアドバイスを求めてください。
妊娠
妊娠中の女性に関する大量のデータ(1,000以上の暴露結果)は、奇形毒性と胎児毒性がないことを示しています。臨床的に必要な場合は、妊娠中にメトクロプラミドを使用できます。 (他の神経弛緩薬と同様に)薬理学的特性のため、妊娠の終わりにメトクロプラミドを投与した場合、新生児の錐体外路症候群を除外することはできません。メトクロプラミドは妊娠の終わりには避けるべきです。メトクロプラミドを使用する場合は、新生児モニタリングを開始する必要があります。
えさの時間
メトクロプラミドは母乳中に低レベルで排泄されます。母乳で育てられた乳児の副作用を排除することはできません。したがって、母乳育児中のメトクロプラミドは推奨されません。母乳育児中の女性におけるメトクロプラミドの中止を検討する必要があります。
機械を運転して使用する能力への影響
メトクロプラミドは、傾眠、めまい、ジスキネジア、ジストニアを引き起こす可能性があり、視力に影響を及ぼし、機械の運転や使用の能力を妨げる可能性があります
投与量と使用方法Plasilの使用方法:投与量
すべての適応症(成人患者)
推奨される単回投与量は10mgで、1日3回まで繰り返すことができます。
推奨される最大1日量は30mgまたは0.5mg / kg体重です。
推奨される最大治療期間は5日です
遅延化学療法誘発性悪心および嘔吐(CINV)の予防(1〜18歳の小児患者)
推奨用量は0.1〜0.15 mg / kg体重で、1日3回まで経口投与できます。 24時間での最大投与量は0.5mg / kg体重です。
投与量表
化学療法誘発性悪心および嘔吐(CINV)の遅延を予防するための最大治療期間は5日です。
指示された用量で、できれば食事の前に薬を投与することをお勧めします。錠剤は体重61kg未満の子供には適していません。
他の剤形/強みは、この集団での投与により適している可能性があります
投与方法:
嘔吐または投与の拒否の場合でも、2回の投与の間の最低6時間の間隔を尊重する必要があります(「特別な警告」のセクションを参照)。
特別な人口
高齢者
高齢患者では、腎機能と肝機能、および一般的な感受性に基づいて用量を減らすことを検討する必要があります。
腎不全
末期腎疾患(クレアチニンクリアランス≤15ml/分)の患者では、1日量を75%減らす必要があります。中等度から重度の腎不全(クレアチニンクリアランス15〜60 ml /分)の患者では、1日量を50%減らす必要があります。
肝不全
重度の肝不全の患者では、用量を50%減らす必要があります。
これらの特定の集団での投与には、他の剤形/強度がより適切である可能性があります。
小児人口
メトクロプラミドは1歳未満の子供には禁忌です(「禁忌」のセクションを参照)。
この製剤は、この集団での投与には適していません
過剰摂取あなたがあまりにも多くのプラシルを服用した場合の対処法
徴候と症状
錐体外路症状、傾眠、意識レベルの低下、錯乱、幻覚、心肺停止が発生する可能性があります。
管理
過剰摂取に関連する、または関連しない錐体外路症状の場合、治療は対症療法のみです(小児のベンゾジアゼピンおよび/または成人の抗コリン作用性抗パーキンソン薬)。
対症療法と心血管機能および呼吸機能の継続的なモニタリングは、臨床状態に基づいて実施する必要があります。
誤って過剰な量のプラミドを摂取/摂取した場合は、すぐに医師に通知するか、最寄りの病院に行ってください。
プラシルの使用について疑問がある場合は、医師または薬剤師に連絡してください
副作用プラシルの副作用は何ですか
すべての薬と同様に、プラシルは副作用を引き起こす可能性がありますが、誰もがそれらを得るわけではありません。副作用は、システムと臓器によって分類されます。周波数は、次の規則を使用して定義されます。
- 非常に一般的(≥1/ 10)、
- 一般的(≥1/ 100から<1/10)、
- 珍しい(≥1/ 1,000から<1/100)、
- まれ(≥1/ 10,000から<1 / 1,000)、
- 非常にまれ(<1 / 10,000)、
- 不明(利用可能なデータから頻度を推定することはできません)。
*高プロラクチン血症(無月経、乳汁漏出、女性化乳房)に関連する長期治療中の内分泌病変。
以下の反応は、高用量が与えられると、より頻繁に発生します。
- 錐体外路症状:特に子供と若年成人において、薬物の単回投与後でも、急性ジストニアとジスキネジア、パーキンソン症候群、アカシジア(「特別な警告」のセクションを参照)。
- 傾眠、意識レベルの低下、混乱、幻覚。
パッケージリーフレットに含まれている指示に準拠することで、望ましくない影響のリスクを軽減できます。
副作用の報告
副作用が出た場合は、医師または薬剤師に相談してください。これには、このリーフレットに記載されていない可能性のある副作用も含まれます。望ましくない影響は、www.agenziafarmaco.gov.it / it / responsabiliの全国報告システムを通じて直接報告することもできます。
副作用を報告することにより、この薬の安全性に関するより多くの情報を提供するのに役立ちます。
有効期限と保持
有効期限:パッケージに印刷されている有効期限を確認してください。表示されている有効期限は、正しく保管された無傷のパッケージに入った製品を指します。
警告:パッケージに記載されている有効期限が切れた後は、薬を使用しないでください。
医薬品は、廃水や家庭ごみとして処分しないでください。使用しなくなった薬を捨てる方法を薬剤師に尋ねてください。これは環境を保護するのに役立ちます。
この医薬品を子供たちの視界や手の届かないところに保管してください
構成
1錠に含まれるもの:
有効成分:メトクロプラミド一塩酸塩一水和物10.5mg(無水物10mg相当)。
賦形剤:グアーガム;メチルセルロース;エチルセルロース;コロイダル水和シリカ;ジャガイモでんぷん;ステアリン酸マグネシウム;ペンタエリスリトール。
剤形および内容物「10mg錠」-24錠
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
プラシル10MG錠
02.0定性的および定量的組成
10mg錠
1錠に含まれるもの:
有効成分:メトクロプラミド一塩酸塩一水和物10.5mg(無水物10mg相当)。
添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形
タブレット
04.0臨床情報
04.1治療適応
成人人口
プラシルは成人に次のように適応されます:
-化学療法誘発性悪心および嘔吐(CINV)の遅延の予防
-放射線療法誘発性の悪心および嘔吐(RINV)の予防
-急性片頭痛誘発性の悪心および嘔吐を含む、悪心および嘔吐の対症療法。メトクロプラミドは、急性片頭痛における鎮痛薬の吸収を改善するために経口鎮痛薬と組み合わせて使用することができます。
小児人口
プラシルは、1〜18歳の子供に次の理由で適応されます。
-セカンドラインオプションとしての遅延化学療法誘発性悪心および嘔吐(CINV)の予防
04.2投与の形態と方法
すべての適応症(成人患者)
推奨される単回投与量は10mgで、1日3回まで繰り返すことができます。
推奨される最大1日量は30mgまたは0.5mg / kg体重です。
推奨される最大治療期間は5日です
遅延化学療法誘発性悪心および嘔吐(CINV)の予防(1〜18歳の小児患者)
推奨用量は0.1〜0.15 mg / kg体重で、1日3回まで経口投与できます。 24時間での最大投与量は0.5mg / kg体重です。
投与量表
化学療法誘発性悪心および嘔吐(CINV)の遅延を予防するための最大治療期間は5日です。
指示された用量で、できれば食事の前に薬を投与することをお勧めします。
錠剤は体重61kg未満の子供には適していません。
他の剤形/強みは、この集団での投与により適している可能性があります
投与方法:
嘔吐または用量の拒絶の場合でも、2回の投与の間に最低6時間の間隔を守る必要があります(セクション4.4を参照)。
特別な人口
高齢者
高齢患者では、腎機能と肝機能、および一般的な感受性に基づいて用量を減らすことを検討する必要があります。
腎不全:
末期腎疾患(クレアチニンクリアランス≤15ml/分)の患者では、1日量を75%減らす必要があります。
中等度から重度の腎機能障害(クレアチニンクリアランス15〜60 ml /分)の患者では、1日量を50%減らす必要があります(セクション5.2を参照)。
肝不全:
重度の肝機能障害のある患者では、用量を50%減らす必要があります(セクション5.2を参照)。
これらの特定の集団での投与には、他の剤形/強度がより適切である可能性があります。
小児人口
メトクロプラミドは1歳未満の子供には禁忌です(セクション4.3を参照)。
この製剤は、この集団での投与には適していません
04.3禁忌
•活性物質またはセクション6.1に記載されている賦形剤のいずれかに対する過敏症
•胃腸の運動性の刺激がリスクをもたらす胃腸出血、機械的閉塞、または胃腸穿孔
•重度の高血圧のエピソードのリスクがあるため、褐色細胞腫が確認または疑われる
•緑内障の患者
•神経弛緩薬またはメトクロプラミドによって誘発された遅発性ジスキネジアの病歴
•てんかん(発作の頻度と強度の増加)
• パーキンソン病
•レボドパまたはドーパミン作動薬との併用(セクション4.5を参照)
•メトクロプラミドによるメトヘモグロビン血症またはNADHシトクロムb5レダクターゼ欠損症の既知の病歴
•錐体外路障害のリスクが高いため、1歳未満の子供に使用します(セクション4.4を参照)。
04.4使用に関する特別な警告と適切な注意事項
神経学的障害
錐体外路障害は、特に子供や若年成人、および/または高用量の使用で発生する可能性があります。これらの反応は通常、治療の開始時に発生し、単回投与後に発生する可能性があります。錐体外路症状の場合は、メトクロプラミドを直ちに中止する必要があります。これらの効果は通常、治療の中止後に完全に元に戻すことができますが、対症療法が必要になる場合があります(小児ではベンゾジアゼピン、成人では抗コリン作用薬および抗パーキンソン薬)。
過剰摂取の場合を避けるために、嘔吐や投与の拒否の場合でも、セクション4.2で指定されているように、2回の投与の間の少なくとも6時間の時間間隔を尊重する必要があります。
メトクロプラミドによる長期治療は、特に高齢者において、潜在的に不可逆的な遅発性ジスキネジーを引き起こす可能性があります。遅発性ジスキネジアのリスクがあるため、治療期間は3か月を超えてはなりません(セクション4.8を参照)。遅発性ジスキネジーの症状が現れた場合は、治療を中止する必要があります。
神経遮断薬悪性症候群は、メトクロプラミドと神経弛緩薬の併用、およびメトクロプラミド単剤療法で報告されています(セクション4.8を参照)。神経弛緩薬悪性症候群の症状の場合は、メトクロプラミドを直ちに中止し、適切な治療を開始する必要があります。
神経障害を併発している患者や、中枢神経系に影響を与える他の薬剤で治療されている患者には、特に注意を払う必要があります(セクション4.3を参照)。
パーキンソン病の症状は、メトクロプラミドによって悪化する可能性があります。
メトヘモグロビン血症
NADHチトクロームb5レダクターゼ欠損症に関連している可能性のあるメトヘモグロビン血症が報告されています。そのような場合、メトクロプラミドは直ちにそして永久に中止されるべきであり、適切な措置(メチレンブルー治療など)が取られるべきです。
心臓の病状
循環虚脱、重度の徐脈、心停止、QT間隔の延長など、深刻な心血管系の望ましくない影響が、特に静脈内に注射可能なメトクロプラミドを投与した後に報告されています(セクション4.8を参照)。
メトクロプラミドを、特に高齢者、心臓伝導障害(QT間隔の延長を含む)の患者、電解質の不均衡、徐脈が矯正されていない患者、およびQT間隔を延長することが知られている他の薬剤を服用している患者に静脈内投与する場合は特に注意が必要です。
静脈内投与は、副作用(例えば、低血圧、アカシジア)のリスクを減らすために、ゆっくりとしたボーラス(少なくとも3分間の持続時間)として与えられるべきです。
腎不全および肝不全
腎不全または重度の肝不全の患者では、用量を減らすことが推奨されます(セクション4.2を参照)。
特に乳がんまたはプロラクチン分泌性下垂体腺腫の患者では、プロラクチンレベルの上昇の可能性を慎重に検討する必要があります。
メトクロプラミドとアルコール飲料の併用はお勧めしません。
04.5他の医薬品との相互作用および他の形態の相互作用
禁忌の関連
レボドパまたはドーパミン作動薬とメトクロプラミドは互いに拮抗します(セクション4.3を参照)。
避けるべき関連
アルコールはメトクロプラミドの鎮静効果を高めます。
考慮すべき関連
メトクロプラミドの運動促進効果により、一部の薬物の吸収が損なわれる可能性があります。
抗コリン作用薬およびモルヒネ誘導体
抗コリン作用薬とモルヒネ誘導体は両方とも、消化管の運動性に対してメトクロプラミドに対して拮抗作用を示す可能性があります。
中枢神経系抑制剤(モルヒネ誘導体、抗不安薬、鎮静H1抗ヒスタミン薬、鎮静抗うつ薬、バルビツール酸塩、クロニジンおよび関連薬)
CNS抑制薬とメトクロプラミドの鎮静効果が増強されます。
神経弛緩薬
メトクロプラミドは、錐体外路障害の場合、他の神経弛緩薬と相加効果がある可能性があります。
セロトニン作動薬
SSRIなどのセロトニン作動薬と一緒にメトクロプラミドを使用すると、セロトニン症候群のリスクが高まる可能性があります。
ジゴキシン
メトクロプラミドは、ジゴキシンの生物学的利用能を低下させる可能性があります。ジゴキシンの血漿中濃度を綿密に監視する必要があります。
シクロスポリン
メトクロプラミドはシクロスポリンの生物学的利用能を増加させます(Cmaxは46%、曝露は22%)。シクロスポリン血漿濃度の綿密なモニタリングが必要です。臨床的影響は不確実です。
ミバクリウムとスキサメトニウム
メトクロプラミドの注射は、神経筋遮断の期間を延長することができます(血漿コリンエステラーゼの阻害を通じて)。
CYP2D6の強力な阻害剤
フルオキセチンやパロキセチンなどの強力なCYP2D6阻害剤と併用すると、メトクロプラミドの曝露レベルが上昇します。臨床的意義は不明ですが、患者は副作用がないか監視する必要があります。
シスプラチン
いくつかの観察は、メトクロプラミドで、シスプラチンの腎毒性の増加を報告しています。
インスリン
メトクロプラミド治療は、食物を含む腸管通過を減らすことにより、糖尿病におけるインスリン投与量の調整を必要とする場合があります。
メトクロプラミドはまた、S.N.C。に対するアポモルヒネの影響を軽減します。
04.6妊娠と授乳
妊娠
妊娠中の女性に関する大量のデータ(1,000以上の暴露結果)は、奇形毒性と胎児毒性がないことを示しています。臨床的に必要な場合は、妊娠中にメトクロプラミドを使用できます。 (他の神経弛緩薬と同様に)薬理学的特性のため、妊娠の終わりにメトクロプラミドを投与した場合、新生児の錐体外路症候群を除外することはできません。メトクロプラミドは妊娠の終わりには避けるべきです。メトクロプラミドを使用する場合は、新生児モニタリングを開始する必要があります。
えさの時間
メトクロプラミドは母乳中に低レベルで排泄されます。母乳で育てられた乳児の副作用を排除することはできません。したがって、母乳育児中のメトクロプラミドは推奨されません。母乳育児中の女性におけるメトクロプラミドの中止を検討する必要があります。
04.7機械の運転および使用能力への影響
メトクロプラミドは、傾眠、めまい、ジスキネジア、ジストニアを引き起こす可能性があり、視力に影響を及ぼし、機械の運転や使用の能力を妨げる可能性があります。
04.8望ましくない影響
副作用は、システムと臓器によって分類されます。頻度は、次の規則を使用して定義されます:非常に一般的(≥1/ 10)、一般的(≥1/ 100、
*高プロラクチン血症(無月経、乳汁漏出、女性化乳房)に関連する長期治療中の内分泌病変。
以下の反応は、高用量が与えられると、より頻繁に発生します。
•錐体外路症状:急性ジストニアおよびジスキネジア、パーキンソン症候群、アカシジア、特に子供および若年成人における単回投与後でも(セクション4.4を参照)。
•傾眠、意識レベルの低下、錯乱、幻覚。
疑わしい副作用の報告。
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスク比の継続的なモニタリングを可能にするため、重要です。医療専門家は、www.agenziafarmaco.gov.it / it / responsabiliの全国報告システムを介して疑わしい副作用を報告するように求められます。
04.9過剰摂取
症状
錐体外路症状、傾眠、意識レベルの低下、錯乱、幻覚、心肺停止が発生する可能性があります。
管理
過剰摂取に関連する、または関連しない錐体外路症状の場合、治療は対症療法のみです(小児のベンゾジアゼピンおよび/または成人の抗コリン作用性抗パーキンソン薬)。
対症療法と心血管機能および呼吸機能の継続的なモニタリングは、臨床状態に基づいて実施する必要があります。
05.0薬理学的特性
05.1薬力学的特性
薬物療法グループ:機能性胃腸障害の薬-運動促進薬
ATCコード:A03FA01
メトクロプラミドは、胃、膵臓、胆汁の分泌を変えることなく、胃腸管の上気道の運動性を刺激し、調整します。
その作用機序は複雑で、D1およびD2受容体(ドーパミン)と5-HT3受容体(セロトニン)の競合的拮抗薬、および腸内コリン作動性ニューロンの刺激に関与する5-HT4受容体の非特異的作動薬です。膣の神経支配とは無関係であるが、アトロピンおよび他のムスカリン拮抗薬によって廃止された腸の運動促進活性。
それは、胃十二指腸収縮の緊張と振幅の増加を決定し、遠位感覚が次第に減少するまで、空腸、回腸、および結腸の推進運動の協調的な増加を決定し、管腔内内容物の末梢進行を伴う。
食道の中部と下部の3分の1の筋肉の緊張をさらに高め、括約筋のレベルの圧力を高めると同時に、幽門と十二指腸の球根を解放します。これらの作用により、胃が空になり、胃が空になります。十二指腸から胃への逆流と食道。
05.2「薬物動態特性
吸収:メトクロプラミドは十分に吸収され、10 mgの単回投与後、約1時間後に54 ng / mlの血漿レベルに達し、異なる経口製剤間で大きなばらつきはありません。その生物学的利用能は35から100%の間で個々に異なります。筋肉内経路は、約3時間で検出される有意に高い濃度ピークを決定します。
分布:薬物は基本的な脂溶性化合物であり、大量の分布(2.2〜3.4 L / Kg / h)と急速な組織破壊があり、製剤の分布半減期は5〜21分です。iv。 (経口の場合は0.35〜0.63時間)。血漿タンパク質との結合親和性は、循環中に存在する量の40%に相当します。
代謝:薬物は単純な抱合プロセスで肝臓で代謝されます。正常な腎機能の存在下での肝機能のわずかな変化は、薬物動態パラメータの明らかな変更の素因とはならないようです。
活性血漿濃度:それらは治療される疾患の性質と重症度に依存します。たとえば、10〜20 ng / mLの値は治療範囲の下限を表しますが、シスプラチンの嘔吐に対抗するには、1000 ng / mLを超える高濃度が必要になる場合があります。
除去:それは用量依存的であり、10および20mgの単回経口投与後3〜5時間の間で変動します。クリアランスは0.4〜0.7 L / kg / hです。
経口投与量の約86%が尿中に排泄され、一部は遊離型、一部は不活性代謝物であり、主なものはN-硫酸塩とN-グルクロン酸であり、残りは胆汁やその他の排出物で排泄されます(メトクロプラミドはまた、牛乳と一緒に排泄されます)。
メトクロプラミドのクリアランスは、腎不全の患者では著しく減少します(0.2 L / kg / h)。
腎不全
メトクロプラミドのクリアランスは、重度の腎不全の患者では最大70%減少しますが、血漿排出半減期は増加します(クレアチニンクリアランスが10〜50 ml /分で約10時間、クリアランスが15時間)のクレアチニン
肝不全
メトクロプラミドの蓄積は肝硬変の患者に見られ、血漿クリアランスの50%の減少に関連していました。
05.3前臨床安全性データ
実験動物のデータは、安全性、反復投与毒性、遺伝子毒性、発がん性、生殖毒性に関する従来の研究に基づくと、ヒトに対する特別な危険性を明らかにしていません。
06.0医薬品情報
06.1添加剤
グアーガム;メチルセルロース;エチルセルロース;コロイド状水和シリカ;ジャガイモでんぷん;ステアリン酸マグネシウム;ペンタエリスリトール。
06.2非互換性
非互換性のケースは強調されていません。
06.3有効期間
3年
06.4保管に関する特別な注意事項
提供されていない。
06.5即時包装の性質および包装の内容
10mgの24錠の箱
06.6使用および取り扱いに関する指示
特別な指示はありません
07.0マーケティング承認保持者
サノフィS.p.A.
Viale L. Bodio 37 / b-IT-20158ミラノ
08.0マーケティング承認番号
10mg錠、24錠:AIC 020766046
09.0最初の承認または承認の更新の日付
03.10.1966/01.06.2010
10.0本文の改訂日
2015年5月








.jpg)



-e-bpco.jpg)