有効成分:スクラルファート
SUCRAMAL 1g錠
Sucramalの添付文書は、パックサイズで利用できます。- SUCRAMAL 1g錠
- 経口懸濁液用SUCRAMAL2g顆粒
なぜスクラマルが使われるのですか?それはなんのためですか?
消化性潰瘍および胃食道逆流症の薬
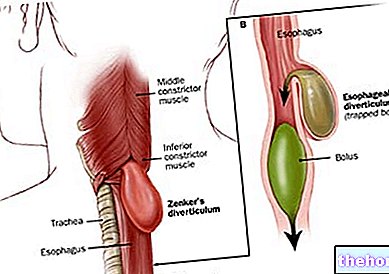
胃潰瘍、十二指腸潰瘍。急性胃炎、慢性症候性胃炎、NSAID胃障害(非ステロイド性抗炎症薬)、逆流性食道炎。
Sucramalを使用すべきでない場合の禁忌
活性物質またはいずれかの賦形剤に対する過敏症。テトラサイクリンによる抗生物質治療中は、抗生物質の不活性化を伴う複雑な塩の形成を避けるために投与しないでください。未熟児にはスクラルファートを投与しないでください。
使用上の注意スクラマルを服用する前に知っておくべきこと
慢性腎不全の患者には、Sucramalを注意して使用する必要があります。このような患者では、吸収されたアルミニウムの排泄が損なわれる可能性があります。妊娠中の使用は慎重に検討し、明らかに必要な場合は予約する必要があります(特別な警告のセクションを参照)。
手術、薬物療法、または運動障害の後に胃腸運動障害のある患者にスクラルファート投与後に胃石が形成されるという報告があります。
スクラルファートを投与された乳児を対象にフランスで実施されたよく知られた研究では、治療を受けた乳児の73%が重度の消化器系の問題を示し、36%が治療を必要とする閉塞症候群を示しました。
市販後調査中に、結果として呼吸器合併症を伴うスクラルファート錠の誤嚥の症例が報告されています。したがって、最近または長期の挿管、気管切開、以前の誤嚥、嚥下障害、または咽頭や咳反射に影響を及ぼしたり、協調や口腔咽頭の運動性を低下させたりする可能性のあるその他の状態など、嚥下を損なう可能性のある状態の患者には、スクラルファート錠剤を注意して使用する必要があります。
テトラサイクリンとのスクラマルの使用は推奨されません(「相互作用」のセクションを参照)。
14歳未満の子供および青年での使用
データが不十分なため、14歳未満の子供にSucramalを使用することはお勧めしません。
どの薬や食品がスクラマルの効果を変える可能性があるか
複雑な塩の形成とその結果としての抗生物質の不活性化を避けるために、テトラサイクリンによる治療中にスクラルファートを投与しないでください。これらの薬の吸収が減少するため、スクラルファートの摂取と他の薬の摂取の間に少なくとも2時間の間隔を空けることをお勧めします。
処方箋がない場合でも、他の薬を服用している、または最近服用したことがあるかどうかを医師または薬剤師に伝えてください。
警告次のことを知っておくことが重要です。
妊娠と母乳育児
妊娠中の女性を対象とした十分に管理された研究はないため、妊娠の際に厳密に必要な場合にのみ使用する必要があります。母乳からスクラルファートが除去されるかどうかは不明ですが、授乳中の製品の投与は注意して行う必要があります。
薬を服用する前に、医師または薬剤師にアドバイスを求めてください。
機械を運転して使用する能力への影響
スクラルファートは、機械の運転や使用に影響を与える可能性のある影響を引き起こしません。
いくつかの成分に関する重要な情報
皮膚の錠剤には、胃の不調や下痢を引き起こす可能性のある硬化ヒマシ油が含まれています。
投与量と使用方法Sucramalの使用方法:投与量
大人
医師の意見では、1錠を1日3〜4回、食事から持ち帰ります。
子供と青年での使用
データが不十分なため、14歳未満の子供にはSucramalの使用は推奨されません。
この薬の使用についてさらに質問がある場合は、医師または薬剤師に相談してください。
過剰摂取スクラマルを飲みすぎた場合の対処方法
ヒトの過剰摂取に関する既知のデータはありません。12g/ kg体重までの用量を使用した動物の急性毒性試験では、致死量を決定することはできませんでした。誤って飲み過ぎた場合は、すぐに医師に相談するか、最寄りの病院に行ってください。
副作用Sucramalの副作用は何ですか
すべての薬と同様に、スクラマルは副作用を引き起こす可能性がありますが、誰もがそれらを手に入れるわけではありません。以下の副作用は、臨床試験および市販後の経験で報告されています。
パッケージリーフレットに含まれている指示に準拠することで、望ましくない影響のリスクを軽減できます。副作用が深刻になった場合、またはこのリーフレットに記載されていない副作用に気付いた場合は、医師または薬剤師にご連絡ください。
有効期限と保持
有効期限:パッケージに記載されている有効期限をご覧ください。有効期間は、正しく保管された無傷のパッケージの製品を対象としています。
警告:パッケージに記載されている有効期限が切れた後は、製品を使用しないでください。薬は廃水や家庭ごみとして処分しないでください。使用しなくなった薬は薬剤師に捨ててください。環境保護に役立ちます。
医薬品を子供たちの手の届かないところに置いてください。
その他の情報
構成
各タブレットには
有効成分:1gスクラルファート
賦形剤:微結晶性セルロース、ブラックチェリーフレーバー、カルメロースナトリウム、硬化ヒマシ油、ステアリン酸マグネシウム。
剤形と内容
錠剤:40錠の箱。
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
SUCRAMAL 1Gタブレット
02.0定性的および定量的組成
1錠には1gのスクラルファートが含まれています。
既知の効果を持つ賦形剤:硬化ヒマシ油。
添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形
タブレット。
04.0臨床情報
04.1治療適応
胃潰瘍、十二指腸潰瘍。急性胃炎、慢性症候性胃炎、NSAID胃障害(非ステロイド性抗炎症薬)、逆流性食道炎。
04.2投与の形態と方法
大人:
医師の意見では、1錠を1日3〜4回、食後に服用します。
小児人口
14歳未満の子供におけるSucramalの安全性と有効性は確立されていません。
現在利用可能なデータはセクション5.1で説明されています。
04.3禁忌
活性物質またはセクション6.1に記載されている賦形剤のいずれかに対する過敏症。
テトラサイクリンによる抗生物質治療中は、結果として抗生物質が不活性化する複合塩の形成を避けるために、スクラルファートを投与しないでください。
未熟児にはスクラルファートを投与しないでください。
04.4使用に関する特別な警告と適切な注意事項
慢性腎不全の患者には、Sucramalを注意して使用する必要があります。このような患者では、吸収されたアルミニウムの排泄が損なわれる可能性があります。
妊娠中の使用は慎重に検討し、明らかに必要な場合は予約する必要があります(セクション4.6を参照)。
集中治療室で治療を受けている重病患者を中心に、スクラルファート投与後の胃石形成の報告があります。ほとんどの患者(スクラルファートが推奨されていない新生児を含む)は、胃石形成の素因となる可能性のある根本的な病状(薬物/外科療法または運動性を低下させる障害による胃内容排出の遅延など)を持っているか、同時に腸内栄養を与えられました。
フランスで実施された、スクラルファートを投与された乳児を対象としたよく知られた研究では、治療を受けた乳児の73%が重度の消化器系の問題を示し、36%が治療を必要とする閉塞症候群を示しました。
市販後調査中に、スクラルファート錠の誤嚥とそれに続く呼吸器合併症の孤立した症例が報告されています。したがって、最近または長期の挿管、気管切開、以前の誤嚥、嚥下障害、または咽頭や咳反射に影響を及ぼしたり、協調や口腔咽頭の運動性を低下させたりする可能性のあるその他の状態など、嚥下を損なう可能性のある状態の患者には、スクラルファート錠剤を注意して使用する必要があります。
テトラサイクリンとのSucramalの使用は推奨されません(セクション4.5を参照)。
いくつかの成分に関する重要な情報:
皮膚の錠剤には、胃の不調や下痢を引き起こす可能性のある硬化ヒマシ油が含まれています。
小児人口:
安全性と有効性に関するデータが不十分なため、14歳未満の子供にSucramalを使用することはお勧めしません。
04.5他の医薬品との相互作用および他の形態の相互作用
テトラサイクリンによる治療中は、抗生物質の不活性化を伴う複雑な塩の形成を避けるために、スクラルファートを投与しないでください。
スクラルファートとフェニトイン、ワルファリン、ジゴキシン、フルオロキノロン系抗生物質(シプロフロキサシンやノルフロキサシンなど)を併用すると、これらの薬剤の吸収率が低下します。したがって、スクラルファートの摂取と他の薬の摂取との間に少なくとも2時間の間隔を空けることをお勧めします。
04.6妊娠と授乳
妊娠中の女性を対象とした十分に管理された研究はないため、妊娠の際に厳密に必要な場合にのみ使用する必要があります。母乳からスクラルファートが除去されるかどうかは不明ですが、授乳中の製品の投与は注意して行う必要があります。
04.7機械の運転および使用能力への影響
スクラルファートは、機械の運転や使用に影響を与える可能性のある影響を引き起こしません。
04.8望ましくない影響
以下の副作用は、臨床試験および市販後の経験で報告されています。
疑わしい副作用の報告
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスクバランスを継続的に監視できるため重要です。医療専門家は、国の報告システムを介して疑わしい副作用を報告するよう求められます。 //www.agenziafarmaco.gov.it/it/responsabili。
04.9過剰摂取
ヒトの過剰摂取に関する既知のデータはありません。12g/ kg体重までの用量を使用した動物の急性毒性試験では、致死量を決定することはできませんでした。
05.0薬理学的特性
05.1薬力学的特性
薬物療法グループ:消化性潰瘍および胃食道逆流症の薬; ATCコード:A02BX02
スクラルファート(ショ糖-8硫酸のアルミニウム塩)の抗潰瘍活性は、胃液分泌によるさらなる攻撃から潰瘍領域を保護することによって決定されます。スクラルファートは酸を中和する能力がごくわずかであり、抗潰瘍作用は原因とは言えません。胃酸の中和に。
特に、臨床薬理学の研究は、スクラルファートが潰瘍部位から放出されるタンパク質と潰瘍形成に付着した複合体を形成することを示しています。
小児集団文献では、主にストレス潰瘍、逆流性食道炎、粘膜炎の予防に関する、小児におけるスクラルファートの使用に関する臨床データは限られています。これらの研究で使用される用量は、1日4回0.5〜1gです。子供の年齢と基礎疾患の重症度であり、大きな安全上の懸念なしに投与されました。データが限られていることを考慮して、14歳未満の子供にスクラルファートを使用することはお勧めしません。
05.2薬物動態特性
スクラルファートは消化管から最小限の量でしか吸収されません。消化管から吸収された微量のスクラルファートは、尿を介して排泄されます。
05.3前臨床安全性データ
ラットに12g / kgおよび4g / kgを皮下および腹腔内に経口投与しても、薬物の投与に起因する致死的なエピソードは生じなかった。 4 g / kg /日を180日間長期投与すると、血液学的および血液化学的変化を引き起こすことなく、ラットの体重増加がわずかに遅くなる可能性があります。催奇形性の影響は観察されていません。
06.0医薬品情報
06.1添加剤
微結晶性セルロース、ブラックチェリーフレーバー、カルメロースナトリウム、硬化ヒマシ油、ステアリン酸マグネシウム。
06.2非互換性
なし。
06.3有効期間
5年。
06.4保管に関する特別な注意事項
特に注意はありません。
06.5即時包装の性質および包装の内容
PVC /アルミニウムラミネートで構成されたブリスター。 1gの40錠が入った箱。
06.6使用および取り扱いに関する指示
特別な指示はありません。
07.0マーケティング承認保持者
シャーパーS.p.A. --Viale Ortles、12-20139ミラノ
08.0マーケティング承認番号
SUCRAMAL 1 g錠、40錠AICn。 025724067
09.0最初の承認または承認の更新の日付
最初の承認日:1985年11月7日
最終更新日:2010年6月1日。
10.0本文の改訂日
2016年6月