一般性
慢性骨髄性白血病(CML)の治療には、病気を長期間管理することができるいくつかの治療オプションが含まれます。定期的な血液検査と骨髄検査、および血液専門医または腫瘍専門医による頻繁な評価により、がんの進行を監視できます。

医学的調査(血球数、細胞遺伝学的および分子的検査)の結果から、以下を理解することができます。
- 時間の経過に伴う治療の有効性の程度と治療への反応の進展;
- 病気が薬剤に反応しなくなった場合(治療への抵抗性)。
モニタリングと治療への反応
病気の経過を正しく監視することは、治療の有効性を検証し、その結果、治療が失敗した場合に迅速に介入できるようにするために不可欠です。
細胞遺伝学的分析および分子生物学的調査は、診断目的と同様に、治療プロトコルへの応答の程度を評価し、治療後の疾患の持続性を強調するためにも使用されます(最小限の残存疾患の研究):
- 完全な血液学的反応:治療が効果を発揮し始めると、白血病細胞の数が減少します。血液学検査では異常なクローンを検出できなくなりましたが、これは細胞遺伝学的分析で可能です。
- 完全な細胞遺伝学的応答:フィラデルフィア染色体(Ph)の存在が、従来の細胞遺伝学的分析(治療に対する応答を監視するための標準的なアプローチ)または蛍光insituハイブリダイゼーション(FISH)によって強調されなくなったときに得られます。 Ph +骨髄細胞。細針吸引骨髄サンプルで行われる細胞遺伝学的分析は、フィラデルフィア染色体に加えて、予後の役割を持つ染色体変化の存在を決定するための唯一の方法でもあります。
- 完全な分子応答:分子分析でハイブリッド遺伝子BCR / ABLの発現を検出できない場合に到達します。この治療法は効果的であることが証明されており、bcr-ablタンパク質の産生を促進する分子信号は非常に低いため、分子検査などの高感度検査でも検出できません。監視されている転写レベルの上昇は、治療に対する反応の喪失を示している可能性があります。
これらの結果の達成は非常に重要な結果を表しています。多くの研究は、完全な細胞遺伝学的および分子的反応を示す患者は、疾患が加速期および/または芽球期に進行することなく、長期間生存する可能性が非常に高いことを示しています。 。
多くの要因が治療の有効性に影響を与える可能性があるため、初期段階では、3、6、12、および18か月後にテストを続行することをお勧めします。
さまざまな治療時間での最適な反応と失敗を定義する臨床研究からこれまでに得られた情報は、患者の正しい管理のために従わなければならないモニタリングスキームの策定につながりました( 欧州白血病-ネット):
血液専門医(または腫瘍専門医)は、特定の臨床例における治療の有効性を検証するためにいくつかの目的を確立することができます。患者は治療に対して異なる反応を示し、すべての患者が予測された期間内に最適な治療マイルストーンに到達できるわけではないためです。 。。
治療オプション
CMLの治療の主な目標は、「完全な分子寛解を達成することです。病気は治療によって制御され(完全に消失しなくても)、生成される病理学的クローンの数は、症状を引き起こさないように十分に制限されます。ほとんどの人はできません。白血病細胞を完全に取り除くと、治療は病気の長期寛解を達成するのに役立ちます。
治療目標には以下が含まれます:
- 慢性骨髄性白血病の症状の発現を制限します。
- 血球数に関連する通常のパラメータを復元します。
- フィラデルフィア染色体陽性白血病細胞(Ph +)および分子シグナル(BCR / ABL転写物)の数を減らします。
- フィラデルフィア+染色体の消失を目指します(完全な細胞遺伝学的応答)。
従来の抗芽球薬
のようないくつかの抗芽球薬 ブスルファン (アルキル化)およびl "ヒドロキシ尿素 (DNA合成の特異的阻害剤)は、特に過去に、慢性期の疾患の細胞減少と制御を達成するために使用されてきました。従来の治療は生活の質の改善をもたらしましたが、病気の自然史を大幅に変えることも、加速/芽球期への進行を防ぐこともできませんでした。
組換えインターフェロンアルファ
1980年代初頭から、 インターフェロン 顆粒球シェアの減少と正常化に加えて、細胞遺伝学的および分子的試験の陰性化の達成を観察することを可能にし、慢性期のより長い期間を誘発し、その結果、加速期および/または芽球期の進化が減少する。インターフェロンアルファは、従来のCML療法の役割を減らしました。この薬剤は、患者の20〜30%で完全な細胞遺伝学的応答を誘発し、特にPh +細胞の増殖シグナルの翻訳を妨害し、細胞増殖腫瘍前駆細胞を阻害します。インターフェロンアルファはまた、白血病細胞の生存に間接的なメカニズムで作用し、それらの細胞接着を減少させ、免疫系の細胞の活性を増幅します。
この薬の使用の制限は、その無視できない毒性によって与えられます。インターフェロンの副作用には、倦怠感、発熱、体重減少が含まれます。達成された結果を改善するために、インターフェロンは他の細胞毒性薬と組み合わされました。インターフェロンとシトシンアラビノシド(ARA-C)の関連のみが、インターフェロン単独よりも優れた結果をもたらすことが示されていますが、明らかな生存上の利点はありません。
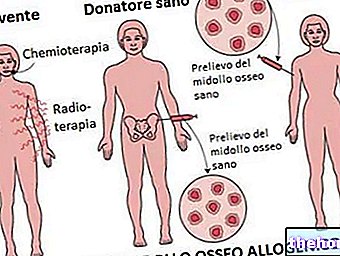
同種骨髄移植
レシピエントと互換性のある健康なドナーからの幹細胞の移植(同種移植)は、何年にもわたって最も頻繁な治療適応症であり、今日でも新生物を確実に根絶することができる唯一の治療法である。
この手順を慢性期に実施すると、約50%の症例で5年間の無病生存率が得られます。
同種骨髄移植は、コンディショニング療法(全身照射と組み合わせた化学療法)によるすべて(またはほぼすべて)のPh +細胞の破壊の最初の段階と、それに続く注入されたドナー幹細胞による造血骨髄の再構成を伴います。さらに、ドナー骨髄リンパ球は、「移植片対白血病」(移植片対白血病)効果と呼ばれる免疫性効果を伴うPh +細胞の制御および/または排除に寄与します。治療への反応は、慢性骨髄性白血病に典型的な分子変化が消失したかどうかを評価することで監視できます。同種骨髄移植は、CMLを「治癒」できる治療法ですが、残念ながら、致命的な毒性や再発による失敗率が伴います。実際、この手順は非常に要求が厳しく、年齢によって影響を受ける可能性があります。患者。患者と移植の早さ(慢性期の診断から数ヶ月または数年):その潜在的な危険性のため、55歳未満の患者にのみ実行可能であり、さらに付随する病状はありません。したがって、同種異系移植は、CMLの少数の患者にのみ真の治療機会を構成します(互換性のある幹細胞ドナーを見つけることの難しさも考慮します)。
最近では、同種移植の対象とならない慢性骨髄性白血病(年齢、ドナーの不足、拒否など)のある被験者において、自家移植が提案されました。 「Ph +細胞(抗芽球+インターフェロンを使用)に対する意図的に適切な細胞破壊療法の後に再注入された患者の骨髄は、Ph-細胞の一般的な再拡張でそれ自体を再構成します。
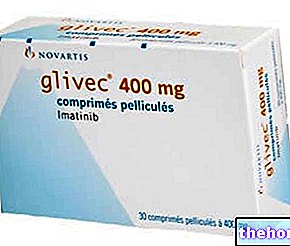
メシル酸イマチニブ(Glivec®)
慢性骨髄性白血病治療の歴史は、患者の生活の質の向上に大きく貢献した最初のチロシンキナーゼ阻害剤(メシル酸イマチニブ)の導入によって革命を起こしました。
イマチニブはBCR / ABLの特異的阻害剤であり、疾患の分子生物学を理解した後に設計され、Ph +慢性骨髄性白血病の治療に使用されます。
この薬は、患者の80〜90%で完全な分子細胞遺伝学的寛解を誘導することができ、好酸球増加症およびPDGRF(血小板由来成長因子、走化性および増殖性を促進する多くの病的状態に関与する血清マイトジェンの関与)を伴う骨髄腫瘍でも活性があります容量)。
イマチニブは、ATPの阻害メカニズムを介してBCR / ABLのチロシンキナーゼ活性を選択的にブロックします。薬剤は、BCR / ABLキナーゼの特定のドメインで利用可能な高エネルギー分子(ATP)に結合し、他の基質のリン酸化を防ぎ、カスケードをブロックします。 Ph +白血病クローンの生成過程に関与するであろう反応の。この分子(メチシル酸イマチニブ)の使用量は、病気の段階と反応に応じて、400mg /日から800mg /日まで変化します。現在、その優れた有効性により、CMLの治療に最適な薬剤です。懸濁液および/または用量の減少で可逆的な副作用は異なる可能性があります(トランスアミナーゼの増加、吐き気、皮膚の発疹、体液貯留など)。
長期にわたって薬剤に対する耐性を示す症例が観察され(例えば、進行した疾患の患者)、治療に対する反応のタイプを定義するための生物学的臨床基準が特定されています。この耐性の原因となるメカニズムは複数あるようです(キナーゼドメインの変異、BCR / ABLの増幅/過剰発現、クローン進化...)。これらの場合、イマチニブ療法を継続することはもはや適切ではありません。
これらの状態の患者の場合、可能なオプションは次のとおりです。
- 同種移植;
- 従来の治療法(ヒドロキシ尿素、ブスルファンなど);
- L "インターフェロン;
- 実験的治療(第2世代チロシンキナーゼ阻害剤による)。
第二世代のチロシンキナーゼ阻害剤
イマチニブ療法の失敗は、加速期および/または芽球期の慢性骨髄性白血病の進行と関連しており、特に予後不良です。近年、薬理学的研究により、臨床診療において、イマチニブに対する耐性を発現した患者に有効な第2世代チロシンキナーゼ阻害剤の使用が可能になりました。ダサチニブ(Sprycel®)およびニロチニブ(Tasigna®)は慢性期の患者に使用されますおよび/またはGlivec®に不応性の進行CMLであり、完全かつ持続的な血液学的、細胞遺伝学的および分子的応答を再誘導することができます。ただし、Ph +クローンは、その遺伝的不安定性のために、 BCR / ABLキナーゼドメインであり、さまざまな阻害薬に耐性があることが証明されています。実験段階の他の分子(第3世代阻害剤)は、慢性骨髄性白血病の特定の標的を対象としています。特に、特定の変異を有する白血病細胞Ph +を感作することができます。 (例:耐性CMLおよびT315I変異を伴うMk-0457は、直接影響を及ぼしますtイマチニブ結合部位)。
「慢性骨髄性白血病治療」に関するその他の記事
- 慢性骨髄性白血病:慢性骨髄性白血病:診断
- 慢性骨髄性白血病:定義、原因、症状